Растворимость - иод
Cтраница 2
Йодистый калий добавляется для повышения растворимости иода. [16]
Бепези и Гильдебрапд [2] установили, что растворимость иода в 7-гепт-форане при 25 составляет 0 0120 % ( вес. Растворимость по закону Рауля должна быть в 1 400 раз больше этой величины. [17]
В присутствии хлористых солей, способствующих значительному повышению растворимости иода в воде, коэффициент распределения иода между органическими растворителями и водой снижается. [18]
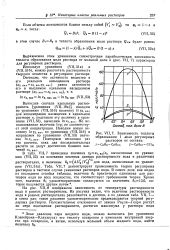
Приводим график ( рис. 69) зависимости логарифма растворимости иода ori / rB различных растворителях. Из этого графика следует, что идеальная растворимость иода, рассчитанная по уравнению Шредера, наблюдается очень редко; только в SnJ4 и в сере, как в растворителях. [19]
Приводим график ( рис. 60) зависимости логарифма растворимости иода от 1 / Т в различных растворителях. Из этого графика следует, что идеальная растворимость иода, рассчитанная по уравнению ( VI, 7), наблюдается очень редко; только в SnI4 и в сере. Но линейная зависимость величины In N от 1 / Т наблюдается во многих растворителях. [20]
В присутствии хлористых солей, способствующих значительному повышению растворимости иода в воде, коэффициент распределения иода между органическими растворителями и водой снижается. [21]
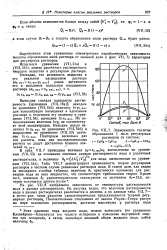
Приводим график ( рис. 57) зависимости логарифма растворимости иода от ЦТ в различных растворителях. [22]
Рекомендуемый способ приготовления основного реактива сберегает время благодаря более быстрой растворимости иода в пиридине по сравнению с его растворимостью в метаноле. Однако, как было указано в предыдущей главе, последовательность прибавления составных частей не оказывает влияния на свойства полученного реактива. [23]
 |
Зависимость теплоты. [24] |
На рис. VI 1 8 изображена зависимость от температуры растворимости иода в разных растворителях. Из рисунка видно, что величины растворимости иода в разных растворителях различаются в десятки, а по данным табл. VII, 7 - в сотни раз; такое различие удовлетворительно предсказывается теорией регулярных растворов. [25]
 |
Зависимость теплоты. [26] |
На рис. VII, 8 изображена зависимость от температуры растворимости иода в разных растворителях. Из рисунка видно, что величины растворимости иода в разных растворителях различаются в десятки, а по данным табл. VII, 7 - в сотни - раз; такое различие удовлетворительно предсказывается теорией регулярных растворев. [27]
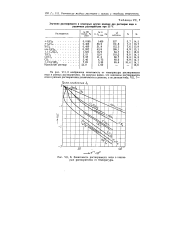 |
Зависимость растворимости иода в некоторых растворителях от температуры. [28] |
На рис. VII, 8 изображена зависимость от температуры растворимости иода в разных растворителях. [29]
Константа скорости адсорбции / из различных солевых растворов остается постоянной, но величина адсорбции оказывается тем выше, чем меньше растворимость иода в данном солевом растворе. Все это находится в полном соответствии с теоретическими представлениями о том, что скорость диффузии растворенных веществ определяется скоростью диффузии молекул растворенного вещества в глубь зерен сорбента. С увеличением объема макропор, являющихся транспортными путями для молекул иода в глубь зерен активированного угля, эта скорость возрастает. Следовательно, процесс адсорбции пода крупнопористыми углями протекает значительно быстрее, чем мелкопористыми. [30]
Страницы: 1 2 3 4