Протонный растворитель
Cтраница 4
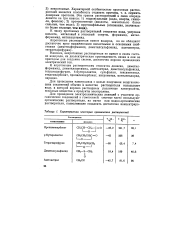 |
Характеристика некоторых органических растворителей. [46] |
К числу протонных растворителей относятся вода, уксусная кислота, метиловый и этиловый спирты, формамид, метил-формамид, метилацетамид. [47]
В качестве неводных протонных растворителей применяют спирты, органические и неорганические кислоты ( серная, фтор-су льфоновая, муравьиная, уксусная, трифторуксусная и др.), аммиак, первичные и вторичные амины, этилендиамин. [48]
В противоположность протонным растворителям апротонные биполярные растворители не нивелируют силу оснований. Катионы стабилизуются в биполярных апротонных растворителях гораздо лучше, чем в протонных. Влияние в общем возрастает с повышением мягкости катионов. [49]
Поэтому в протонных растворителях на сольватации анионов сильно сказываются ион-дипольное взаимодействие и водородная связь. В апротонных растворителях, например в диметил-сульфоксиде, водородная связь отсутствует и сольватация анионов ослаблена. Размеры катионов обычно меньше размеров анионов. Поэтому первые более склонны к диполь-дипольному взаимодействию. На это взаимодействие накладывается комплексообразование, которое можно рассматривать как разновидность сольватации и которое вносит значительный вклад в энергию сольватации. [50]
Кислород в протонном растворителе образует промну ЕОДО о связь, лагэдаря ч - му его нуклеофильность падает. [51]
F в протонных растворителях противоположен ряду возрастания их основности в той же среде - Когда в молекуле нуклеофила возможно взаимодействие с орби-талями неподеленной пары электронов соседнего атома, мягкость-реагента и его нуклеофильность увеличиваются, хотя основность-под влиянием - / - эффекта снижается. Так, реагенты ROO L RSS, RNHNH2 более нуклеофильны и менее основны, чем RO, RS, RNH2 соответственно. [52]
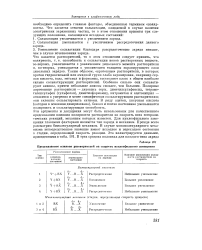 |
Предсказанное влияние растворителей на скорость нуклеофильного замещения. [53] |
Таким образом, протонные растворители, в которых протон гидроксильной или амидной групп слабо экранирован, например серная кислота, вода, метанол и формамид, составляют класс в общем наиболее сильно сольватирующих растворителей. Особенно сильно они сольвати-руют анионы, причем небольшие анионы сильнее, чем большие. Полярные апротонные растворители - двуокись серы, диметилсульфоксид, тетраме-тиленсульфон ( сульфолан), диметилформамид, нитрометан и ацетонитрил - относятся к умеренно и менее специфически сольватирующим растворителям; они склонны сольватировать катионы. В ряду ацетон, уксусная кислота которая в основном димеризована), бензол и гептан постепенно уменьшаются полярность и сольватирующая способность. [54]
Страницы: 1 2 3 4