Реактив - жирар
Cтраница 2
Для удаления примесей, которые могут реагировать с реактивами Жирара, третичнобутиловый спирт предварительно очищают, обрабатывая раствором 2 4-динитрофенилгидразина с последующей перегонкой. Получение производных и разложение под действием формальдегида ведется как описано выше. В этом растворителе получен почти количественный выход с реактивом Жирара - Т для н-алканалей, н-алк-2 - еналей и н - 2 4-диеналей. Реакционную смесь оставляют при обычной температуре на ночь или нагревают в течение часа на водяной бане / Полученный 2 4-динитрофенилгидразон извлекают четыреххлористым углеродом. [16]
Ледерер [32] указывает, что альдегиды весьма быстро реагируют с реактивами Жирара - Р и Т, причем реакция идет в этиловом спирте даже в отсутствие уксусной кислоты. [17]
Остаток после промывания, высушивания и упаривания эфирного раствора с помощью реактива Жирара разделяют на кетон-ную и спиртовую фракции. [18]
 |
Бактерицидная активность тиофеновых производных реактива Жирара Т ( мкг / мл. [19] |
Для выяснения влияния роли величины триалкиламмониевого фрагмента были получены дериваты с реактивом Жирара Т 25, а также производные со специально полученными реактивами Жирара 27 - 30, которые были проверены на бактерицидную активность. Все указанные производные обладали значительно более низкой бактерицидной активностью, монотонно убывающей с ростом величины радикалов при аммонийном азоте. Наивысшую активность проявили производные 2-ацетил - 3-метил - 4 5-дифенилтиофена, поэтому углубленно изучалась активность только этого соединения. [20]
Некоторое количество нспрореатпровавшего кетопа, присутствующего в реакционной смеси, нужно удалять реактивом Жирара Р, кроме того, выход был невысоким. Однако метилциклопропилкетон совершенно инертен по отношению к надбаионной кислоте. [21]
Рейхштейн 2б отметил, что кетоны типа холестанона легко вступают во взаимодействие с реактивом Жирара, образуя гидразоны, которые гидролизуются под действием очень разбавленных минеральных кислот. Соединения типа холестенона тоже легко образуют производные Жирара, но для гидролиза требуются значительно более концентрированные кислоты. Альдегиды реагируют с образованием гидразонов, настолько трудно поддающихся гидролизу кислотами, что этим путем удается полностью отделить кетоны от альдегидов; эффективного метода регенерации альдегидов еще не найдено. Ди-арилкетоны чрезвычайно медленно взаимодействуют с реактивом Жирара. [22]
Хенбест и Джонс27 отметили случаи, когда при отделении кето-стероидов от некетонных стероидов с помощью реактива Жирара в метанольных или этанольных растворах уксусной кислоты производные аллилового спирта, не содержащие кетогрупп, превращаются в соответствующие метиловые или этиловые эфиры. [23]
Ацетон удобно определять в виде Шиффовых оснований с глицином [48], бутиламином [50], семикарбазидом [51], реактивом Жирара - Т [52] и другими аминами. [24]
Таким образом, для рассмотренных производных тиофена, при прочих равных параметрах, определяющим является липофильность тиофеновой части молекулы, а модификация ее реактивами Жирара приводит к обратным результатам - с увеличением величины радикала при аммонийном азоте активность падает. [25]
Соединение LX было превращено ( бромирование, обработка иодидом натрия в ацетоне и восстановление) в ацетат 16 ( 5-фтор-гидрокортизона ( LXI), который был подвергнут очистке с помощью реактива Жирара. [26]
Другой путь изучения кетонной фракции мочи был предложен Вольфом, Гершбергом и Физером341, показавшими, что содержащиеся в нейтральных экстрактах 17-кетостероиды можно определить с точностью до 10 у путем конденсации их с реактивом Жирара и полярографического анализа реакционной смеси в водном буферном растворе. Кетостероиды не мешают определению 17-кетостероидов, поскольку жираровские производные циклогексанона, в отличие от соответствующих производных циклопентанона, не восстанавливаются на ртутном капельном электроде. Кетостероиды характеризуются потенциалом полуволны, равным - 1 4в; а, ( 3-непредельные кетоны, для которых потенциал равен - 1 1 в, могут определяться одновременно с предельными соединениями в том же самом образце. Этим же методом может быть определен также и эстрон. Полярографический метод определения 17-кетостероидов мочи был проверен и усовершенствован рядом других авторов. Вертессен и Бекер3 13 предложили новый способ записи полярографической волны; Барнетт, Генли и Моррис341 ввели усовершенствование, давшее удовлетворительные, результаты при серийных анализах и заключающееся в окислении экстракта мочи перманганатом для разрушения веществ, мешающих определению. [27]
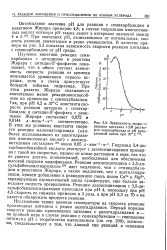 |
Зависимость скорости реакции цитидина с2М раство. [28] |
Изучение кинетики реакции семи-карбазида с цитидином и реактива Жирара с цитидин-5 - фосфатом показывает, что в обоих случаях зависимость скорости реакции от времени описывается уравнением первого порядка, если в смеси присутствует большой избыток гидразида. При этом реактив Жирара оказывается значительно менее реакционноспособ-ным по сравнению с семикарбазидом. Так, при рН 4 2 и 37 С константа скорости реакции цитидина с семикарбазидом и цитидин-5 - фосфата с реактивом Жирара составляет 0 072 и 0 0144 л моль 1 ч - 1 соответственно. [29]
Из других производных гидразина для синтеза соответствующих гидразонов часто используется семикарбазид NH2NHCONH2; получающийся при этом гидразон называется семикарбазоном. Применяются также реактивы Жирара Т и Р, дающие растворимый в воде гидразон, что обусловлено присутствием в нем ионной группы. Часто с помощью реактивов Жирара производят очистку карбонильных соединений. [30]
Страницы: 1 2 3 4