Реакция - инициирование
Cтраница 1
Реакции инициирования удобно подразделять также по структуре первичных инициирующих частиц, вне зависимости от механизма их образования. К А - ]; 2) цвиттер-ионы [ К - А - ]; 3) ион-радикалы К; 4) координационные комплексы, но имеющие ярко выраженного ионного характера. Все эти первичные инициирующие частицы обладают различной активностью в К. В одной и той же системе, в зависимости от условий инициирования, возможно одновременное образование первичных частиц различной структуры или же переход одних частиц в другие в ходе К. [1]
Реакции инициирования удобно подразделять также по структуре первичных инициирующих частиц, вне зависимости от механизма их образования. К А - ]; 2) цвиттер-ионы [ К - А - ]; 3) ион-радикалы К; 4) координационные комплексы, не имеющие ярко выраженного ионного характера. Все эти первичные инициирующие частицы обладают различной активностью в К. В одной и той же системе, в зависимости от условий инициирования, воч-можно одновременное образование первичных частиц различной структуры или же переход одних частиц в другие в ходе К. [2]
Реакция инициирования при дисперсионной полимеризации осуществляется как в частицах, так и в дисперсионной среде. Однако, учитывая высокие скорости захвата радикалов частицами, формально можно относить скорость инициирования к объему полимерных частиц. [3]
Реакции инициирования и роста требуют переноса двух протонов от аммонийной соли к азоту лактама одновременно с открытием лактамного кольца. [4]
Реакции инициирования, роста, передачи и обрыва цепи подобны соответствующим стадиям в гомогенных и гетерогенных реакциях химической ( со) полимеризации [ 16, с. На эти реакции оказывает влияние электрическое поле электрода, которое изменяет скорость и степень ( со) полимеризации. Это явление особенно проявляется в случае ионного механизма ( со) полимеризации [ 16, с. Часто электродные процессы сопровождаются явлениями адсорбции и десорбции различных веществ на поверхности электрода, включая молекулы мономера и активные центры. Этим реакции электрохимической ( со) полимеризации отличаются от классических ( со) по-лимеризационных реакций. [5]
Реакция инициирования при повышении температуры на 10 С ускоряется приблизительно в 2 - 3 раза. Учитывая, что эта реакция является определяющей, суммарная скорость радикальной полимеризации также будет увеличиваться с повышением температуры. [6]
Реакция инициирования заключается в переводе молекул мономера в активное состояние, при котором она способна к реакции полимеризации. Это достигается термическим воздействием ( термополимеризация), действием света ( фотополимеризация), радиоактивным облучением ( радиационная полимеризация), действием катализаторов ( BF3, A1C13 и др.) и перекисей. [7]
Реакция инициирования имеет первый порядок по мономеру, а реакция роста - близкий к нулевому. [8]
Реакция инициирования является сильно эндотермичной. [9]
Реакции инициирования объяснены еще не полностью. Они могут протекать как в результате непосредственного взаимодействия молекулярного кислорода с углеводородом, так и под каталитическим воздействием ионов тяжелых металлов. Автокаталитическое окисление может быть целенаправленно инициировано пероксидами. В то время как для насыщенных углеводородов места образования радикалов в молекулярной цепи случайны ( статистическое расположение), для олефинов образование радикалов происходит в энергетически более выгодных местах: по метиленовым группам в а-положении к двойной связи или по подвижному атому водорода. Реакция роста молекулярной цепи (3.16) практически не нуждается в энергии активации. Гидропероксиды распадаются с образованием радикалов и вызывают каталитическую лавину. При этом протекание реакции описывается экспоненциальным законом. [10]
Реакция инициирования вызывает образование начальных активных центров и определяет общую скорость полит меризации. Инициирование полимеризации начинается с распада на свободные радикалы соединений, содержащих лабильные связи типа - О-О -, - S-S - и другие, энергия диссоциации которых находится в пределах 85 - 210 кДж / моль. К таким соединениям относятся гидроперекиси, диалкильные и диацильные перекиси, перкислоты, перэфиры, перкарбонаты, полиперекиси, персульфаты, триазены, азосоединения, дисульфиды и ряд других. [11]
 |
Введение способных к со-полимеризации групп в полимер путем сополимеризации с бифункциональным мономером ( а или путем введения ре-акционноспособных центров ( б. [12] |
Реакции инициирования, роста цепи и прививки представлены следующей схемой. [13]
Реакция инициирования радикальной полимеризации заключается в образовании первичного активного свободного. [14]
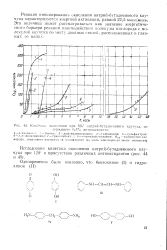 |
Кинетика окисления при 120 натрий-бутадие. ювого каучука. [15] |
Страницы: 1 2 3 4