Реакция - карбонилирование
Cтраница 2
Скорость реакции карбонилирования значительно выше, чем окисления, поэтому активность катализатора с течением времени падает. Для ускорения реакции окисления металлического палладия используют водные растворы хлоридов меди и железа, которые являются активными переносчиками кислорода и быстро переводят образующийся в результате реакции карбонилирования металлический палладий в хлорид палладия. [16]
В реакцию карбонилирования могут быть вовлечены первичные, вторичные, третичные спирты, а также диолы. Вторичные и третичные спирты реагируют легче первичных. [17]
В реакциях карбонилирования, помимо минеральных кислот, применены в качестве катализаторов галоидные соли никеля или карбо-нилы Ni и Со, или же комплексные соединения этих металлов. [18]
Рассмотренные выше реакции карбонилирования ни в какой мере не исчерпывают этой области. Реакции карбонилирования могут проходить также со спиртами, простыми эфирами линейного и циклического строения и лактонами. [19]
При помощи реакции карбонилирования можно получить столько карбоновых кислот ( со всеми их производными), сколько есть олефиновых углеводородов. При рассмотренных условиях получаются следующие продукты: из диалкилэтиленов, например нзобутилена, получаются главным образом изовалерьяновая и триметилуксусная кислоты ( см. стр. [20]
При условиях реакции карбонилирования стирол полимеризуется с образованием небольших количеств кислотных продуктов. [21]
Возможности использования реакции карбонилирования в органическом синтезе еще далеко не исчерпаны. Имеющиеся данные показывают, что существует много других интересных областей применения этой реакции. [22]
Подавляющее большинство реакций карбонилирования органических соединений протекает в присутствии катализаторов, которые можно разделить на три основные группы: кислотные ( минеральные кислоты, BFs и его комплексы), основные ( неорганические основания) и соединения переходных металлов. Из них наибольший теоретический и практический интерес представляет последняя группа катализаторов. Несмотря на огромный эмпирический материал, накопленный за последние 30 - 40 лет в области каталитического синтеза с участием окиси углерода, основной трудностью, встречающейся при разработке новых и усовершенствовании существующих процессов, является отсутствие надежных критериев подбора катализаторов реакции. Наиболее подробно изучен механизм гидроформи-лирования олефинов в присутствии карбонилов металлов VIII группы периодической системы. Карбонилирование других классов химических соединений исследовано менее детально. Однако имеющийся экспериментальный материал позволяет выявить общие закономерности реакции карбонилирования, понять химизм процесса и наметить направления поиска эффективных катализаторов. [23]
К этим реакциям карбонилирования примыкают реакции циклизации ацетиленов в производные бензола и цик-лооктатетраена. [24]
 |
A. MMH. 3Hlte кобальтовых солей органических кислот. [25] |
Показано, что реакция карбонилирования в присутствии кобальтовых солей органических кислот протекает на такую же глубину, как с карбонилами кобальта. [26]
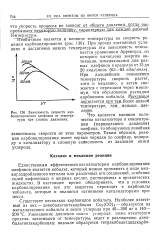 |
Зависимость скорости кар - Ле - Ш6. [27] |
Таким образом, реакция карбонилирования имеет первые порядки по олефину, водороду и катализатору и сложную зависимость от давления окиси углерода. [28]
Область возможного применения реакций карбонилирования ни в коей мере не ограничивается ацетиленовыми углеводородами и олефинами. Эту реакцию с окисью углерода возможно проводить также со спиртами, сложными эфирами, ациклическими и циклическими простыми эфирамн и лаптопами в присутствии катализаторов - соединений никеля или кобальта и галоидов, например иода, при повышенных температурах и давлениях. [29]
Присутствие в продуктах реакции карбонилирования цис - и гранс-изомеров MeCOMn ( CO) 4L показано с помощью ЯМР - и ИК-спектров. [30]
Страницы: 1 2 3 4