Реакция - катализатор
Cтраница 1
Гидрообессеривающая реакция катализатора является важнейшей, так как при любых вариантах и условиях процесса достаточно полное обессеривание продуктов является обязательным условием. Все реакции гидрообессеривания экзотермичны. [1]
При реакции катализатора с молекулами мономера образуются ионы с отрицательным зарядом. При дальнейшем взаимодействии образовавшихся ионов происходит рост цепи с передачей по цепи отрицательного заряда. Одновременно увеличивается молекулярная масса полимера. Обрыв цепи, видимо, связан с присоединением к ней положительного заряда. [2]
Введением в зону реакции катализаторов можно сильно изменить направление крекинга. Так, например, на некоторых катализаторах удается с хорошими выходами получать из предельных углеводородов олефины или диолефины ( стр. В присутствии хлористого алюминия усиленно идут процессы изомеризации. [3]
Введением в зону реакции катализаторов можно сильно изменить направление крекинга. Так, например, на некоторых катализаторах удается с хорошими выходами получать из предельных углеводородов олефины или диолефины ( стр. В присутствии хлорида алюминия усиленно идут процессы изомеризации. [4]
Введением в зону реакции катализаторов можно сильно изменить направление крекинга. [5]
Из применявшихся в этой реакции катализаторов - окись алюминия [1, 2], алюмосиликаты, окись хрома на окиси алюминия [3], окись тория на окиси алюминия - наилучшим является последний, введенный в практику Репе: выход пирролидина достигает 80 % при снижении температуры реакции до 300 - 320 С. [6]
В ряде случаев скорости реакций катализатора ( I) и ( II) могут быть определены вне катализа. Иначе обстоит дело, если превращения катализатора происходят при участии реагентов каталитической реакции. [7]
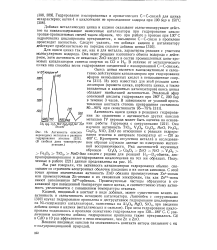 |
Активность окислов переходных металлов в реакции гидрирования этилена. ( В скобках даны температуры реакции. [8] |
Из всех известных для этой реакции катализаторов ( хромита цинка, карбоната цинка, а также ванадиевых и кадмиевых катализаторов) окись цинка обладает наибольшей активностью. Этиловый эфир олеиновой кислоты гидрировали при 280 С, 200 бар в течение 3 часов. [9]
Широкое варьирование соотношений количеств взятых в реакцию катализатора и диенофила, как правило, не сказывается на результатах диеновой конденсации. [10]
Так, двухвалентная медь, образующаяся в реакции катализатора - одновалентной меди ( см. выше) с гидроперекисями, в присутствии антиокислителя восстанавливается в одновалентную, и катализ возобновляется. В отсутствие антиокислителя он может прекратиться, так как двухвалентная медь окисления не ускоряет. В товарных топливах, не подвергавшихся глубокой очистке, особенно содержащих продукты вторичных процессов переработки нефти, практически всегда присутствуют небольшие примеси соединений, играющих роль природных антиокислителей ( фенолы, некоторые серосодержащие соединения, смолистые вещества), поэтому окисление топлив в условиях хранения и применения ускоряется металлами. [11]
Мономер в некоторых случаях принимает участие в реакциях катализатора. В результате присоединения первого мономерного звена к активному центру происходит инициирование каталитической полимеризации. [12]
Предпринято несколько попыток связать активность в этих реакциях катализаторов разного состава с некоторыми физико-химическими параметрами. В одной из таких работ [328] рассматривается связь каталитической активности окисных систем Bi O3 - МоО3, Fe2O3 - МоО3, Со2О3 - МоО3, Fe2O8 - Sb2O4, Co2O4 - SbaO4 и SnO2 - Sb2O4 в реакциях полного окисления олефинов с подвижностью кислорода в решетке ( оцениваемой по энергии активации Е0 изотопного обмена кислорода решетки с молекулярным кислородом), с работой выхода электрона ( Аф) и электропроводностью ( а) катализатора. [13]
Основная особенность контакторов - постоянное присутствие в зоне реакции катализатора в виде отдельных кусков, зерен ( гранул) или песка. Как известно, катализатор, ускоряя химическую реакцию, сам в ней участия не принимает. Однако каталитическое действие его с течением времени падает, так как продукты реакции постепенно покрывают пленкой поверхность частиц катализатора, общая поверхность контакта уменьшается и реакция идет все медленнее. Кратковременные повышения температуры в работающем реакторе часто приводят к чрезмерному уплотнению и даже спеканию катализатора. Гидравлическое сопротивление в зоне реакции повышается, что вызывает уменьшение доступа реакционной смеси. Иногда катализатор ( металлический) выполняют в виде проволочных сеток, которые устанавливают в несколько рядов на пути движущегося продукта. Во время работы такие сетки покрываются пленкой окиси. Пленка постепенно становится все толще, отделяя катализатор от реакционной массы. [14]
В ряде случаев указанные растворители принимают участие в реакциях катализатора, что позволяет активно воздействовать на их направление и глубину. [15]
Страницы: 1 2 3 4