Реакция - крекинг - кумол
Cтраница 2
Шваб объясняет природу каталитической активности цеолитов в реакции крекинга кумола [8] ненасыщенностью электроотрицательных ( анионных) центров, возникающих при замещении одновалентного Na па двувалентный катион. Повышение энергии активации при переходе от Mg к Zn автор объясняет более сильным поляризующим действием иона. Авторы считают, что, кроме кислотных центров, для крекинга необходимо второе условие - наличие на поверхности отрицательно заряженных центров - оснований Льюиса. [16]
Туркевич и др. [78] изучали отравление хинолином реакции крекинга кумола на декатионированных молекулярных ситах. После предварительной обработки катализаторов в реактор поочередно вводились импульсы хинолина и кумола. Импульсы хино-лина полностью адсорбировались, и крекинг кумола служил мерой активности катализатора. Хотя такая методика очень проста, распределение яда в этом случае не известно. [17]
Для того чтобы установить истинное кинетическое уравнение реакции крекинга кумола, были проведены опыты с применением дифференциального реактора в условиях, которые исключали все три источника неточностей, указанные выше. [18]
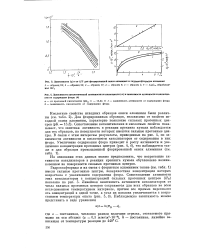
В работе [8] изучалось изменение энергии активации реакции крекинга кумола и р-кумола ( псевдокумола) при 500 на цеолите типа X в зависимости от природы замещающего катиона и степени замещения им иона Na. Из рисунка видно, что замещение в цеолите NaX катиона Na на двухвалентные катионы ( Mg и Са) почти вдвое снижает энергию активации реакции, замещение иона Na на Zn, Mn снижает энергию активации при тех же степенях замещения заметно меньше, введение Cd, наоборот, увеличивает энергию активации. Значения энергии активации проходят через минимум. [19]
Вначале рассмотрим результаты, полученные при изучении реакции крекинга кумола в присутствии дейтерированного алюмосиликатного катализатора. [20]
В присутствии кислотных ( декатионированных) цеолитных катализаторов реакция крекинга кумола протекает с участием карбо-ний-ионов. [21]
Из данных этих авторов следует, что для уменьшения реакции крекинга кумола практически до нуля требуется 1 27 - 1017 молекул хинолина на 1 м2 поверхности. [22]
Ранее в наших работах [1-11] было установлено, что в реакциях крекинга кумола, дегидратации спиртов, полимеризации изобутилена, дисмутации этилбен-зола, алкилирования толуола пропиленом и этиловым спиртом каталитически активным является алюминий в состоянии четверной координации. [23]
Влияние фтористого бора на каталитическую активность окиси алюминия и алюмосиликатов для реакции крекинга кумола и дегидратации этилового спирта. [24]
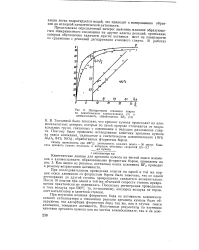
Сопоставление каталитических и кислотных свойств показывает, что заметная активность в реакции крекинга кумола наблюдается для тех образцов, на поверхности которых имеются сильные протонные центры. В связи с этим интересны результаты, приведенные на рис. 4, по зависимости активности и кислотности катализаторов от содержания в них фтора. [26]
 |
Дегидратация этилового спирта. [27] |
При изучении влияния фтористого бора на активность алюмосили-катного катализатора в отношении реакции крекинга кумола было обнаружено, что адсорбция фтористого бора так же, как в случае окиси алюминия, повышает - активность. [28]
На основании этих данных можно предположить, что возрастание активности катализаторов в реакции крекинга кумола обусловлено возникновением на поверхности сильных протонных центров. [29]
Облучение алюмосиликатного катализатора протонами и улучами увеличивает его активность в значительной степени в реакции крекинга кумола, а также в реакции полимеризации изоамиленов. [30]
Страницы: 1 2 3 4