Реакция - ацеталирование
Cтраница 2
Невидимому, реакция ацеталирования протекает по всем указанным схемам. [16]
По мере продвижения реакции ацеталирования диспергированный продукт все в большей мере переходит в раствор, образуя прозрачный спиртовой раствор поливинилацеталя. Ацеталь в дальнейшем может быть выделен осаждением водой. Этот вариант редко применяется, невидимому, из-за сложных операций осаждения, а также необходимости регенерации растворителей и отделения побочных продуктов. По существу он не имеет никаких преимуществ перед обычным однованным методом. [17]
По мере продвижения реакции ацеталирования диспергированный продукт все в большей мере переходит в раствор, образуя прозрачный спиртовой раствор полн-винилацеталя. Ацеталь в дальнейшем может быть выделен осаждением водой. Этот вариант редко применяется, повпдимому, из-за сложных операций осаждения, а также необходимости регенерации растворителей и отделения побочных продуктов. По существу он не имеет никаких преимуществ перед обычным однованным методом. [18]
При указанной температуре реакцию ацеталирования проводят 3 - 4 часа до образования прозрачного раствора поливинилфор-маля. [19]
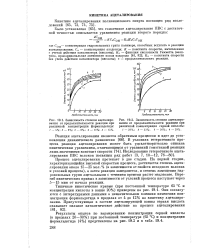
Серная кислота является катализатором реакции ацеталирования поливинилового спирта. Сульфат натрия вводится в состав ацеталирующей ванны для снижения набухаемости волокна и уменьшения возможности склеивания волокон. Температура обработки составляет 60 - 70 С, продолжительность обработки - 25 - 30 мин. В этих условиях с формальдегидом реагирует 30 - 40 % от общего количества групп ОН, находящихся в поливиниловом спирте. Формализация происходит преимущественно в аморфных участках волокна. Чем выше суммарное число прореагировавших групп ОН при внутри - и межмолекулярном ацеталировании, тем выше теплостойкость волокна, характеризуемая величиной усадки в кипящей воде. [20]
 |
Течение реакции формализации волокна из поливинилового спирта, предварительно стабилизованного нагреванием при 210 в течение 7 мин. [21] |
При формализации не стабилизированного волокна реакция ацеталирования охватывает и кристаллические зоны. После формализации винилоновое волокно подвергается промывке и сушке. [22]
По второму варианту двухванного метода реакцию ацеталирования ведут в водном растворе поливинилового спирта. По мере продвижения реакции полимер становится нерастворимым и выпадает из водного раствора. Такой процесс может быть назван водно-гетерогенным ацеталированием поливинилового спирта. Он был разработан С. Н. Ушаковым с сотрудниками для всех видов ацеталей поливинилового спирта. [23]
Таким образом, микроволновое излучение также интенсифицирует реакции ацеталирования. [24]
Поэтому для образования этих групп были использованы реакции ацеталирования и дегидратации поливинилового спирта. [25]
Строение исходного ПВС также влияет на скорость реакций ацеталирования и гидролиза. [26]
Сон - концентрация гидроксильных групп полимера, способных вступить в реакцию ацеталирования; Са - концентрация альдегида; К - константа скорости, вычисленная с учетом действия катализатора ( кислоты); Н0 - функция кислотности Гамметта ( величина, пропорциональная активности ионов водорода [81, 82]; К0 - константа скорости без учета действия катализатора ( кислоты); т - продолжительность реакции. [28]
Увеличение содержания серной кислоты в ванне ( рис. 1) в первую очередь способствует протеканию реакции ацеталирования, при концентрации серной кислоты 25 % и выше процесс привитой сополиконденсации практически вообще прекращается. С увеличением содержания катализатора в ванне наблюдается значительное снижение привеса волокна, тогда как его обменная емкость, отвечающая содержанию фенольных гидроксилов ( Еон) [9] в рабочем диапазоне концентрации серной кислоты в ванне от 5 до 20 %, сохраняется практически на одинаковом уровне ( 1.2 - 1.3 мг-экв. Волокна, полученные по вышеуказанному режиму, отличаются высокой скоростью ионного обмена, стойки к щелочам и кислотам, имеют хорошие прочностные показатели. [29]
Протеканию этой реакции способствуют антипирены и кислоты Льюиса, при распаде которых образуются кислоты, катализирующие реакцию ацеталирования. В этом случае исчезновение гидр-оксильных групп происходит без потерь массы. Рассмотренный механизм пиролиза возможен при термической обработке в инертной среде целлюлозы, предварительно окисленной йодной кислотой до диальдегидцеллюлозы. Исследование механизма пиролиза диальдегидцеллюлозы представляет интерес. [30]
Страницы: 1 2 3 4