Реакция - развитие - цепь
Cтраница 3
Реакции развития цепи прекращаются, и цепь обрывается в результате уничтожения свободных радикалов за счет их рекомбинации в молекулу. Различные радикалы и атомы обладают различной активностью, и поэтому вещества имеют разную скорость развития цени и, следовательно, различную длину цепи. В тех случаях, когда радикалы весьма активны и быстро реагируют с молекулами, длина цепи даже при комнатной темп-ре может быть очень большой. В таких случаях цепь при комнатной темп-ре будет очень короткой и может даже совсем отсутствовать, если рекомбинация радикалов происходит с большей скоростью, чем реакции развития цепи. [31]
Скорость же реакции развития цепи, определяющая вероятность перехода процесса в режим взрыва, зависит как от концентрации стабилизированных атомов брома и условий теплообмена, так и от интенсивности облучения. При достаточно малой интенсивности скорость развития цепи может оказаться недостаточной для перехода реакции в режим взрыва. [32]
Как мы уже указывали, для такого типа реакций мало различаются предэкспоненциальные множители констант скоростей. Если же реакции развития цепи состоят из стадий, включающих не только реакции замещения, но и реакции присоединения, то в этих случаях для определения наиболее медленной стадии необходимо учитывать различие не только в энергиях активации, но и в стерических факторах. Мы видели в главе I, что реакции присоединения атомов или радикалов к двойной связи идут замедленно вследствие очень малых, в сравнении с реакциями замещения, стерических факторов. [33]
Как мы уже указывали, для такого типа реакций мало различаются предэкспонснциалыше множители констант скоростей. Если же реакции развития цепи состоят из стадий, включающих не только реакции замещения, но и реакции присоединения, то в этих случаях для определения наиболее медленной стадии необходимо учитывать различие не только в энергиях активации, но ив стерических факторах. Мы видели в главе I, что реакции присоединения атомов или радикалов к двойной связи идут замедленно вследствие очень малых, по сравнению с реакциями замещения, стерических факторов. Это может привести к тому, что наиболее трудной элементарной стадией может оказаться реакция присоединения по двойной связи, несмотря на то, что ее энергия активации меньше энергии активации других стадий цепи. [34]
Реакциями развития цепи могут быть реакции присоединения радикалов по кратной связи, реакции перехода атома или радикала, в простейшем случае - реакции Н - перехода, а также реакции изомеризации радикалов. В этой и последующей главах обсуждаются реакции развития цепи. Начнем с реакций Х - перехода и рассмотрим вначале экспериментальные кинетические данные. [35]
Полимеризация в этом случае протекает иначе, чем линейная полимеризация или полимеризация с катализаторами или без них. Разветвленные линейные цепи, которые получились вследствие реакции развития цепи в присутствии хлористого алюминия, вызывают побочные реакции циклизации с последующим разрывом. Метод получения этих смазочных масел широко применяется в промышленности. [36]
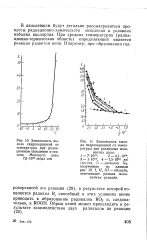
В дальнейшем будут детально рассматриваться процессы радиационно-химического окисления в условиях избытка кислорода. При средних температурах ( радиа-ционно-термическая область) определяющей является реакция развития цепи. [38]
В этой схеме реакция ( 6) является реакцией инициирования цепи. Реакции ( 7) и ( 8) представляют собой реакции развития цепи, а реакция ( 9) - реакцию обрыва цепи. [39]
Здесь юр и Л 0 - скорости реакций развития цепи и суммарные скорости рекомбинации и диспропорционирования радикалов, которые могут быть измерены на опыте. Правая часть, соотношения ( 159) характеризует относительное значение константы скорости реакции развития цепи. [40]
Таким образом, цепные реакции состоят из ряда параллельно-последовательных процессов с участием свободных атомов и радикалов. Всякое цепное превращение включает реакции трех типов: реакцию зарождения цепи, реакцию развития цепи и реакцию обрыва цепи. [41]
Для объяснения этого рассмотрим механизм деполимеризации ( стр. Как видно из схемы реакции, к образованию наиболее летучих продуктов - мономеров приводит реакция развития цепи; продукты распада с более высоким молекулярным весом образуются по реакции передачи цепи. Очевидно, что реакция по схеме 3 протекает преимущественно у полимеров, не имеющих заместителей, например, у полиэтилена и у содержащих подвижный атом водорода. Ароматическая группа повышает активность полимерных радикалов. [42]
Значительно более детальная картина простого процесса полимеризации, получается при рассмотрении истинных значений констант скорости реакций развития цепи и обрыва ее. К сожалению, эти величины нельзя получить из измерений суммарной кинетики, так, хотя 7 в уравнении ( 9) можно часто-определить независимо, но kp и kt не удается разделить. Вместо этого необходимо провести исследования при специальных условиях, при которых не существовало бы концентрации радикалов устойчивого состояния, например фотоиндуцируемая полимеризация под воздействием неустойчивого источника света. Этот метод, впервые предложенный Чэпменом, Брайерсом и Уолтерсом [31], но лишь недавно примененный, к реакциям полимеризации [15, 27], оказался наиболее плодотворным. Его часто описывают как метод вращающегося сектора после обычных средств изменения интенсивности инициирующего реакцию света. Хотя принцип его прост и понятен из приведенных ниже объяснений, но практическое применение его может оказаться довольно сложным. [43]
В тех случаях, когда радикалы, ведущие цепь, мало активны, скорость взаимодействия их с молекулами исходных веществ оказывается того же порядка, как и скорость их рекомбинации. При этом цепи будут короткими или совсем мбгут отсутствовать, если скорость рекомбинации радикалов окажется больше скорости реакции развития цепей. Если в молекулах замедлителей имеются легко рвущиеся связи, то радикал или атом, ведущий цепь, сталкиваясь с такой молекулой, погибает, а вместо него образуется малоактивный радикал, из-за чего цепь обрывается и цепная реакция развиваться в таких условиях не может. [44]
В приведенной схеме горения метана реакция 1 получения радикала метила ( СН3) из атомарного водорода ( Н -) является реакцией зарождения цепи. Реакции получения радикала гидропероксида метила ( 2), гидропероксида метила и радикала метила ( 3), метилового спирта и радикала метила ( 5), воды и радикала метила ( 6), радикала НО2 ( 7), метальдеги-да, радикала гидроксила и воды ( 8) являются реакциями развития цепи. [45]
Страницы: 1 2 3 4