Реакция - рекомбинация
Cтраница 3
Обратная образованию радикалов реакция рекомбинации их может произойти в том случае, когда радикал продиффундирует в клетку, в которой находится второй радикал. [31]
При последующем изучении реакций рекомбинации и диспропорционирования этильных радикалов [289] в различных условиях было показано, что при низких давлениях начинают играть заметную роль реакции радикалов на стенках, а при высоких давлениях - тримолекулярные реакции в объеме. [32]
Сложность зоны протекания реакции рекомбинации является следствием относительно большого процентного содержания исходных реагентов, необходимого для поддержания стабильного пламени. [33]
Из последних двух реакций рекомбинации следует, что величина сигнала сильно зависит от концентрации воды. Поэтому при количественном анализе важно знать, не находится ли анализируемый компонент вблизи области элюирования воды, возможно присутствующей в пробе в довольно больших количествах. В описанной ситуации хвост пика воды, трудно устранимый в большинстве колонок, может наложиться на важный в аналитическом отношении участок хроматограммы. [34]
Значения энергий активации реакций рекомбинации для радикалов RO2 различной структуры также различаются. [35]
Из-за ожидаемой быстроты реакций рекомбинации и диспропорционирования бирадикала невозможно различить эти альтернативные механизмы путем использования обычного метода захвата радикалов. [36]
Изучению зависимости скорости реакции рекомбинации рздикз-лов - СН3 от давления посвящен ряд работ. При давлениях ниже 1 33 - Ю3 Па происходит изменение порядков: порядок реакции рекомбинации становится третьим, а реакции диссоциации - вторым. Граничное давление сильно зависит от температуры, и при 900 К изменение порядков реакций происходит уже при 1 06 - Ю5 Па. Кинетика реакций (5.2) при низких давлениях обсуждена в гл. [37]
При интенсивное протекании реакции рекомбинации цепного воспламенения может вообще не произойти. В реакции горения газообразного топлива основную роль играет тепловое воспламенение. Явления теплового воспламенения горючей смеси пли ее потухания определяются тепловыми режимами реакций. [38]
При большой затрудненности реакции рекомбинации водородных атомов ( 528) и электрохимической десорбции ( 529) увеличивается возможность растворения Надс в металле и последующей диффузии водорода в глубь металла ( см. рис. 174), что часто приводит к появлению водородной хрупкости металла. [39]
Обрыв цепи осуществляется реакцией рекомбинации. [40]
Обрыв цепей осуществляется реакцией рекомбинации. [41]
Обрыв цепи осуществляется реакцией рекомбинации. [42]
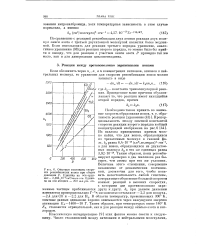 |
Опытные константы скорости рекомбинации ионов при общем давлении Р. Единица на оси орди. [43] |
По сравнению с реакцией рекомбинации двух атомов реакция двух молекул окиси азота с третьей двухатомной молекулой является более медленной. Если использовать для реакции третьего порядка уравнение, аналогичное уравнению ( 98) для реакции второго порядка, то можно было бы прийти к выводу, что для реакции с участием окиси азота Р примерно так же мало, как и для димеризации циклопентадиена. [44]
Изменения соотношений между реакциями рекомбинации и диспропорционирования радикалов свидетельствуют о том, что активность радикалов определяется не только строением самого радикала, но и условиями окружения. Абсолютная активность радикалов может быть оценена лишь в таких условиях, когда у радикалов нет возможности реагировать со средой или передавать ей энергию. Эти условия могут быть осуществлены лишь в высоком вакууме, когда длина свободного пробега радикалов велика и соударения происходят в основном с такими же радикалами. [45]
Страницы: 1 2 3 4