Реакция - взаимодействие - водород
Cтраница 3
При таком соотношении парциальных давлений при 700 К самопроизвольно будет протекать не образование HI, а его разложение. Таким образом, реакция взаимодействия водорода с иодом должна проходить не до конца, а только до определенного предела, точно так же, как и реакция разложения чистого HI идет до некоторого предела. [31]
Газ, загрязнен ный примесью кислорода и воды, через ротаметр поступает в очиститель, в котором находится палладированный силикагель, нагретый в печи до 300 С. Палладированный силикагель служит катализатором реакции взаимодействия водорода с кислородом. Имеющийся в газе кислород соединяется с водородом, образуя воду. [32]
В результате этих исследований было показано, что наибольшей каталитической активностью ( удельной) в отношении реакции взаимодействия водорода и кислорода обладают металлы группы VIII периодической системы элементов Д. И. Менделеева: никель, платина и палладий. При этом для обеспечения реакции взаимодействия водорода и кислорода при температурах порядка 30 - 40 С и высоких объемных скоростях ( до 10000 ч - 1) необходим такой катализатор, который обеспечивал бы протекание процесса в области внешней диффузии. Температура катализатора должна подниматься ка 15 - 20 выше температуры конденсации водяного пара, так как в противном случае активность катализатора может быть резко понижена. [33]
 |
Кривая поглощения ЯМР ( протонов этилового спирта.| Спектры ЭПР атомов Н и О свободных радикалов ОН, OD. [34] |
На рис. ПО показан спектр ЭПР атомов водорода и кислорода, а также свободных радикалов ОН. Такие спектры обнаруживаются при исследовании реакций взаимодействия водорода с кислородом. Это подтверждает, что реакция между Н2 и О2 протекает по цепному механизму через образование свободных радикалов. [35]
Полагая, что константа равновесия реакции взаимодействия водорода и кислорода сильно сдвинута в сторону образования [ ОН ], можно рассчитать количество водорода, ушедшего из раствора в результате взаимодействия с известным количеством кислорода. Далее с помощью графика на рис. 1 можно рассчитать соответствующее этому количеству водорода изменение электрического сопротивления и сравнить его с наблюдаемым в эксперименте. [36]
Никелевые катализаторы более пирофорны, чем железные, что обусловлено большей теплотой хемосорбции кислорода, а также тем, что адсорбированный на никеле водород может окисляться при контакте с воздухом. Ввиду того, что на никеле реакция взаимодействия водорода с кислородом протекает уже при комнатной температуре, пассивация никелевых катализаторов, в отличие от. [37]
Выбор пути, по которому протекает процесс взаимодействия, определяется энергиями активации его элементарных актов. В - табл. 13 приведены энергии активации реакций взаимодействия водорода с галогенами. Энергия активации молекулярной реакции Н2 12 - - 2Н1 равна 168 кдж / моль. [38]
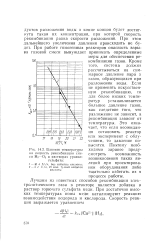 |
Влияние температуры на скорость рекомбинации смеси Н2 - О2 в растворах уранил-сульфата. [39] |
Лучшим из известных способов рекомбинации электролитического газа в реакторе является добавка в раствор горючего сульфата меди. При достаточно высоких температурах ионы меди катализируют реакцию взаимодействия водорода и кислорода. [40]
Небольшой избыток водорода резко уменьшает равновесное парциальное давление кислорода. При небольшом избытке водорода и нагрева до 1000 С реакция взаимодействия водорода с кислородом может рассматриваться как необратимая. Для катализа может быть использован палладиевый катализатор ( цилиндры высотой 10 мм и диаметром 5 мм, покрытые палладием), активность которого, непосредственно связанная с поверхностью, при избытке кислорода резко понижается. [41]
При анализе причин автолегирования силановым методом обычно считают газовую среду химически нейтральной. Однако в работах [ 6, 71, посвященных исследованию реакций взаимодействия водорода со свободными гидридообразующими элементами ( в газообразном и твердом состоянии), было показано, что вполне возможно прямое образование гидридов. По способности прямого гпдрпдообразования при высоких температурах интересующие нас элементы располагаются в следующем порядке: Р, Si, As, В, Sb. [42]
В предыдущей главе элементарные реакции были определены как такие, в которых превращение реагентов в конечные продукты совершается в одну стадию через единственный активированный комплекс. Как уже было показано, к элементарным реакциям можно отнести реакцию взаимодействия водорода и иода, протекающую с образованием йодистого водорода. Реакции, осуществляющиеся через несколько элементарных стадий, как, например, реакция разложения этана, являются сложными. Следующая глава целиком посвящена сложным реакциям, а в этой рассматриваются элементарные реакции и те процессы, которые являются отдельными стадиями сложных реакций. [43]
При определении оптимальных условий осуществления процессов тонкой каталитической очистки газов в некоторых случаях необходимо учитывать возможность изменения каталитических свойств контактов под воздействием компонентов реакционной смеси. К - Борескова с сотрудниками по исследованию каталитической активности металлов в отношении реакции взаимодействия водорода с кислородом 2 - 5 ] установлено, что в случае непористого никелевого контакта при увеличении концентрации кислорода выше 0 1 % при 180 С резко снижается активность и изменяется порядок реакции по кислороду от первого к нулевому, причем, чем ниже температура, тем лри меньших концентрациях кислорода наступает этот критический переход. В случае же пористого катализатора критический переход не наступает даже при концентрациях кислорода до 2 - 2 5 % и температурах выше 40 С. Это обусловлено тем, что контактный процесс в таких условиях протекает в области внешней диффузии. [45]
Страницы: 1 2 3 4