Реакция - восстановление
Cтраница 2
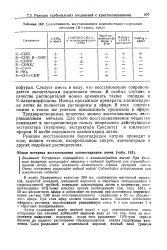 |
Селективность восстановления комплексными гидридами металлов ( Калкил, арил. [16] |
Реакции восстановления борогидридом натрия проводят в воде, водном этаноле, изопропиловом спирте, ацетонитриле и других подобных растворителях. [17]
Реакция восстановления цинком с добавкой едкого натра проходит в растворе в сольвент-нафте при кипении растворителя быстро и гладко. [18]
Реакция восстановления катализируется йодистоводородной кислотой, образующейся за счет взаимодействия йодистого калия с серной кислотой. [19]
Реакции восстановления с LiAlH4 проводятся аналогично реакциям Гриньяра. Для серии аналогичных опытов целесообразно готовить раствор впрок. Для осветления растворов ЫА1Н4 применяют отстаивание в стеклянных цилиндрах или фильтрование в атмосфере азота. [20]
 |
Восстановление триэтоксиалюмогидридом натрия. [21] |
Реакции восстановления триэтоксиалюмогидридом натрия проводятся в диэтиловом эфире или тетрагидрофуране. [22]
Реакции восстановления с помощью А1Н3 до сих пор изучены мало. [23]
Реакция восстановления водородом закиси-окиси железа, в отличие от восстановления им окиси меди, слабо эндотермична, а поэтому обратима. Если пропускать ток водорода над раскаленным окислом железа, получается металлическое железо, а часть водорода обращается в воду. Если, наоборот, через раскаленное металлическое железо пропускать водяные пары, получается окисел железа, а водяные пары частично восстанавливаются в свободный водород. В этих условиях реакции становятся необратимыми потому, что в первом случае ток водорода увлекает с собой образующиеся при реакции водяные пары; во втором случае, наоборот, ток водяных паров увлекает с собой образующийся при реакции водород. И в том и в другом случае возможность обратной реакции исчезает, так как участвующие в ней вещества чисто механически разобщаются. [24]
Реакция восстановления протекает бурно, и при быстром введении формальдегида возможно выбрасывание жидкости. В ходе реакции коричневый цвет раствора переходит в темный сине-зеленый. Для определения полноты восстановления отбирают несколько миллилитров раствора, нагревают, прибавляют NH4OH до слабого запаха аммиака, и доведя до кипения, оставляют для осаждения Сг ( ОН) 3; если раствор над осадком не имеет желтой окраски, восстановление закончено. [25]
Реакции восстановления окислов металлов газами, так же как и окисления металлов, принадлежат к типу гетерогенных топохи-мических реакций. [26]
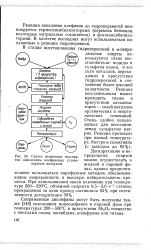 |
Синтез вторичных изоспир-тов окислением олефиновых углеводородов воздухом. [27] |
Реакция восстановления может проходить также в присутствии катализаторов - солей металлов органических и неорганических оснований. Очень удобно пользоваться для восстановления сульфатом натрия. Дегидратацию а-не-предельных спиртов можно осуществлять в жидкой и паровой фазах, однако предпочтительнее пользоваться парофазным методом, обеспечивающим непрерывность и высокую избирательность процесса. [28]
Реакция восстановления 4Н - 3 1-бензоксазин - 4-онов в литературе описана недостаточно подробно. [29]
Реакции восстановления протекают медленно. [30]
Страницы: 1 2 3 4