Реакция - электровосстановление
Cтраница 4
Метод скрытых предельных токов водорода для установления стехиометрии реакции электровосстановления ( в основном, гало-генорганических соединений) наиболее систематически и успешно применял Феоктистов [20, 33-36], который вывел и проверил приведенные уравнения для различных случаев. [46]
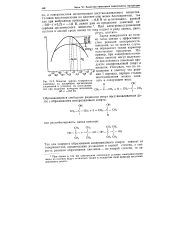 |
Влияние заряда поверхности электрода на адсорбцию органических соединений в условиях их восстановления при заданном катодном потенциале ( 0 8 В. [47] |
Заряд поверхности не только тесно связан с эффективностью реакции электровосстановления, но во многих случаях определяет также характер получаемых продуктов. Например, при электровосстановлении ацетона могут получаться два основных конечных продукта: изопропиловый спирт и пинакон. [48]
Еще большее значение приобретают адсорбционные явления в случае реакций электровосстановления и электроокисления органических веществ. Без учета адсорбции было бы невозможно объяснить часто наблюдаемый кажущийся дробный порядок реакции электровосстановления. Известно, что дробный порядок характерен для гетерогенно-каталитических процессов, протекающих е участием адсорбированных веществ. Дробный порядок отражает разницу между их объемными и поверхностными концентрациями. В связи с этим интересно отметить, что показатель степени у объемной концентрации ацетона оказался одним и тем же и в кинети-чееком уравнении, описывающем процесс его электровосстановле-пия на ртутном катоде, и в уравнении Фрейндлиха, описывающем адсорбцию ацетона на ртути. Такой результат в сочетании с данными, полученными при изучении влияния рН на кинетику процесса, позволил установить, что реакция электровосстановления ацетона на ртути в растворах кислот является реакцией первого порядка как по ацетону, так и по ионам водорода. Протекание реакций электровосстановления через стадию адсорбции более вероятно и энергетически более выгодно даже в тех случаях, когда заполнение поверхности частицами деполяризатора очень мало. [49]
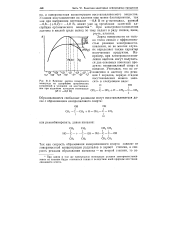 |
Влияние заряда поверхности сать в следующем виде электрода на адсорбцию органических. [50] |
Заряд поверхности не только тесно связан с эффективностью реакции электровосстановления, но во многих случаях определяет также характер получаемых продуктов. Например, при электровосстановлении ацетона могут получаться два основных конечных продукта: изопропиловый спирт и пинакон. [51]
Изложенная здесь концепция, по которой для протекания реакции электровосстановления обязательно требуется участие промежуточно образующихся адсорбированных атомов водорода ( и подобным жо образом для реакций электроокислепия атомов кислорода или поверхностных окислов), исторически восходит к широко распространенному в начале XIX века взгляду па водород и кислород как на универсальные первичные продукты электролиза водных растворов. Так, по Якоби, в медноцинковом элементе выделение меди вызывается действием выделяющегося водорода на сернокислую медь, а растворение цинка рассматривается как растворение окиси цинка, образующейся благодаря окислению металлического цинка выделяющимся кислородом. [52]
Нами собраны и частично рассчитаны стандартные электродные потенциалы реакций электровосстановления некоторых органических веществ, электровосстановление которых исследовано наиболее обстоятельно. [53]
Еще большее значение приобретают адсорбционные явления в случае реакций электровосстановления и электроокисления органических веществ. Без учета адсорбции было бы невозможно объяснить часто наблюдаемый кажущийся дробный порядок реакции электровосстановления. Известно, что дробный порядок характерен для гетерогенно-каталитических процессов, протекающих с участием адсорбированных веществ. В дробном порядке находит свое отражение разница между их объемными и поверхностными концентрациями. В связи с этим интересно отметить, что показатель степени у объемной концентрации ацетона оказался одним и тем же и в кинетическом уравнении, описывающем процесс его электровосстановления на ртутном катоде, и в уравнении Фрейндлиха, описывающем адсорбцию ацетона на ртути. Такой результат в сочетании с данными, полученными при изучении влияния рН на кинетику процесса, позволил установить, что реакция электровосстановления ацетона на ртути в растворах кислот является реакцией первого порядка как по отношению к ацетону, так и по отношению к ионам водорода. [54]
Еще большее значение приобретают адсорбционные явления в случае реакций электровосстановления и электроокисления органических веществ. Без учета адсорбции было бы невозможно объяснить часто наблюдаемый кажущийся дробный порядок реакции электровосстановления. Известно, что дробный порядок характерен для гетерогенно-каталитических процессов, протекающих с участием адсорбированных веществ. В дробном порядке находит свое отражение разница между их объемными и поверхностными концентрациями. В связи с этим интересно отметить, что показатель степени у объемной концентрации ацетона оказался одним и тем же и в. Фрейндлиха, описывающем адсорбцию ацетона на ртути. Такой результат в сочетании с данными, полученными при изучении влияния рН на кинетику процесса, позволил установить, что реакция электровосстановления ацетона на ртути в растворах кислот является реакцией первого порядка как по ацетону, так и по ионам водорода. Протекание реакций электровосстановления через стадию адсорбции более вероятно и энергетически более выгодно даже в тех случаях, когда заполнение поверхности частицами деполяризатора очень мало. [55]
Еще большее значение приобретают адсорбционные явления в случае реакции электровосстановления и электроокисления органических веществ. Без учета адсорбции было бы невозможно объяснить часто наблюдаемы. Известно, что дробный порядок характерен для гетерогенно-каталитичегких процессов, протекающих с участием адсорбированных веществ. Дробный порядок отражает разницу между их объемными и поверхностными концентрациями. В связи с этим интересно отмстить, что показатель степени у объемной концентрации ацетона оказался одним и тем же и в кинетическом уравнении, описывающем процесс его электровосстановле-пия па ртутном катоде, и в уравнении Фрейндлиха, описывающем адсорбцию ацетона на ртути. Таой результат в сочетании с данными, полученными при изучении влияния рН на кинетику процесса, позволил установить, что реакция электровоеетановления ацетона на ртути в растворах кислот является реакцией пе. Протекание реакции электровозегаповлеппя через стадию адсорбции более вероятно и энергетически более выгодно даже в тех случаях, когда заполнение поверхности частицами деполяризатора очень мато. [56]
Страницы: 1 2 3 4