Реакция - алкилирование - ароматические углеводород
Cтраница 3
Такова, например, открытая Ипатьевым и Пайнесом [16] реакция алкилирования ароматических углеводородов, про-мотируемая щелочноорганическими соединениями, стр. При алкилировании бензола этиленом выход этилбензола выше выхода изомерных этилбутилбензолов при реакции этилена с трет. ПайнесиМарк [17] заметили, что реакции алкилирования жирно-ароматических углеводородов всегда идут в направлении, соответствующем наибольшей ионной устойчивости первичных карбанионов по сравнению со вторичными и особенно с третичными. [31]
В последние годы стали успешно применять в качестве катализаторов реакции алкилирования ароматических углеводородов олефинами и спиртами. [32]
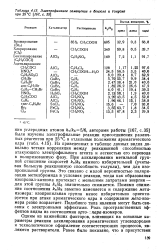 |
Электрофильное замещение в бензоле и толуоле при 25 С [ 167, с. 35 ]. [33] |
Одним из важнейших факторов, влияющих на основные параметры реакции алкилирования ароматических углеводородов и технологическое оформление соответствующих процессов, являются растворители. [34]
Результаты исследования [54] показывают, что алюмосиликатные катализаторы способны ускорять реакцию алкилирования ароматических углеводородов олефинами и парафинами в широком интерволе температур и давлений, а также реакции крекинга боковых цепей алкилароматических углеводородов. [35]
Соединение BFs HsPO / i, кроме высокой каталитической активности в реакции алкилирования ароматических углеводородов олефинами, имеет ряд других очень важных преимуществ и не только по сравнению с молекулярными соединениями фтористого бора, но и с другими, известными катализаторами для этой реакции. [36]
К сожалению, несмотря ыа огромное количество затраченного труда на изучение реакции алкилирования ароматических углеводородов, имеется сравнительно немного кинетических данных по этой реакции. [37]
Для проверки сказанного выше, а также из-за отсутствия в литературе кинетических исследований реакции алкилирования ароматических углеводородов олефинами в присутствии комплекса А1С1з СНзМО2 была проведена настоящая работа. [38]
В обеих написанных выше реакциях употребляются количества хлористого алюминия значительно большие, чем при реакциях алкилирования ароматических углеводородов, это объясняется тем, что в случае получения кетонов кислородсодержащие реагенты, как Хлорангидриды и ангидриды кислот, образуют с эквивалентным количеством хлористого алюминия комплекс. Сами получающиеся в реакции кетоны образуют также комплексы с эквивалентным количеством хлористого алюминия. Эти комплексы во многих случаях хорошо охарактеризованы. Некоторые авторы рассматривают их как соли оксония. [39]
Одним из замечательных свойств катализатора BF j Н3Р04 является то, что при применении его в реакции алкилирования ароматических углеводородов олефинами он не смешивается ни с реагентами, ни с продуктами алкилирования; легко отделяется от них в нижнем слое и может применяться для последующих опытов, так как не отравляется и не теряет заметно своей первоначальной активности. [40]
Путаницу в вопрос о приоритете Г. Г. Густавсона внес своей статьей Е. П. Троицкий [314], который без оснований пытается приписать Г. Г. Густавсону открытие реакции алкилирования ароматических углеводородов в присутствии галогенидов алюминия. [41]
Фирмой Union Carbide Со ( США) предложен новый катализатор SK-500 [412], который относится к типу Y, для проведения реакции алкилирования ароматических углеводородов олефина-ми или галоидалмилами. [42]
Гидриды щелочноземельных металлов при их применении в качестве промоторов имеют то преимущество перед щелочными металлами и их гидридами, что они не катализируют реакцию алкилирования ароматических углеводородов, служащих реакционной средой, этиленом, пропиленом и другими мономерами. Они не катализируют также такие реакции полимеризации этилена или реакции конденсации, в результате которых образуются окрашенные полимерные материалы, а дают чистые белые твердые продукты. [43]
В предлагаемой книге обобщены обширные литературные данные и полученные авторами результаты многолетней работы, позволяющие сделать выводы о современном состоянии теоретических разработок и тенденциях практического использования реакции алкилирования ароматических углеводородов. [44]
Алкильные группы можно ввести в ароматическое ядро следующими способами: реакцией Вюрца-Фиттига или Зайцева-Гриньяра; аци-лированием ароматических углеводородов с последующим восстановлением образующихся алкиларилкетонов; алкилированием ароматических углеводородов галоидными алкилами, спиртами, простыми и сложными эфирами, парафинами или олефинами в присутствии катализаторов H2S04, H3P04, HF, ZnCl2, А1С13, FeCl3 BF3 и др. Из всех этих способов наибольший интерес, несомненно, представляет реакция алкилирования ароматических углеводородов олефинами. Эта реакция обеспечена дешевым и доступным сырьем, осуществляется по сравнительно простой технологической схеме и позволяет получить целевые продукты - алкил-ароматические углеводороды с хорошими выходами. Все это ставит ее вне конкуренции со всеми другими указанными выше способами и обеспечивает ей прекрасные перспективы дальнейшего развития. [45]
Страницы: 1 2 3 4