Реакция - дезаминирование
Cтраница 3
Этот витамин принимает участие в декарбоксилировании щавелевоуксусной кислоты, в реакциях дезаминирования и де-карбоксилирования некоторых аминокислот. [31]
Таким образом, образование сероводорода из цистеина может происходить в результате реакций дезаминирования или переаминирования с последующим превращением 3-меркапто-пировиноградной кислоты в пировиноградную кислоту и серу или сероводород. При наличии избытка цистеина сера перейдет в сероводород; при исследовании цистеиндесульфгидразной реакции наблюдали одновременное превращение цистеина в ци-стин. Интересно отметить, что цистеиндесульфгидразная реакция не идет до конца; в большинстве опытов реакция прекращалась после образования пировиноградной кислоты и сероводорода в количестве, не достигающем половины теоретического. [32]
Присутствие фенильной группы при азоте резко снижает склонность к кольцевому замыканию и сильно повышает возможность реакции дезаминирования. Так же трудно образуется р-нафтилтиодигидроурацил путем нагревания р-нафтил-р-аланина с роданатом калия в присутствии соляной кислоты. Промежуточно образующуюся тиоуреидокислоту выделить не удалось. [33]
Особое место среди процессов, приводящих к карбкатионам, способным к различного рода перегруппировкам, занимает реакция дезаминирования. [34]
В организме человека подвергается распаду около 70 г аминокислот в сутки, при этом в результате реакций дезаминирования и окисления биогенных аминов освобождается большое количество аммиака, являющегося высокотоксичным соединением. Поэтому концентрация аммиака в организме должна сохраняться на низком уровне. В опытах на кроликах показано, что концентрация аммиака 3 ммоль / л является летальной. Таким образом, аммиак должен подвергаться связыванию в тканях с образованием нетоксичных соединений, легко выделяющихся с мочой. [35]
Однако реакция 3 3-диметил - 1-бутиламина - 1 - С14 ( а) с азотистой кислотой показывает, что не все реакции дезаминирования первичных аминов протекают с промежуточным образованием циклических соединений. В результате этой реакции наряду с 2 3-диметилбутанолом - 2 образуется 3 3-диметилбутанол - 1 ( б), причем С14 не перемещается. [36]
Окись алкена, которую не удается выделить в данных условиях реакции, была получена синтетическим путем; при обработке кислотой в условиях реакции дезаминирования она превращается в ту же смесь гликолей и кетонов, что и аминоспирт. [37]
Глутаминовая кислота, являющаяся исходным веществом в этих синтезах, синтезируется, вероятно, из а-кетоглутаровой кислоты под действием L-глутамино-дегидразы в результате обращения приведенной выше реакции дезаминирования. [38]
С точки зрения изучения механизма реакции перегруппировок эти реакции дезаминирования, особенно реакции с аминоспиртами, представляют особый интерес не потому, что они, как все реакции дезаминирования азотистой кислотой, происходят при низкой температуре, а потому, что азот может отщепляться только от углерода, связанного с аминогруппой, тогда как при дегидратации соответствующих гликолей меч то, занятое отщепляющимся гидроксилом, может быть спорным. [39]
Механизм непрямого дезаминирования при участии глютамикодегидро-геназы, кетоглютаровой кислоты и глютамикоаминоферазы, обнаруженный А. Е. Браунштейном, объясняет, каким путем может происходить дезами-нирование природных аминокислот в тканях, несмотря на слабую активность оксидаз аминокислот, катализирующих реакцию прямого дезаминирования этих аминокислот. [40]
Тиамин является составной частью некоторых ферментов ( декарбокси-лаз и дегидрогеназ), катализирующих реакции декарбоксилирования пиро-виноградной и некоторых других органических кислот, а также аминокислот, а биотин принимает участие в декарбоксилировании щавелевоуксусной кислоты и в реакциях дезаминирования и декарбоксилирования некоторых аминокислот. Таким образом, сера играет важную роль в углеводном и азотном обмене в растениях. [41]
Механизм непрямого дезаминирования при участии глютаматдегидро-геназы, кетоглютаровой кислоты и глютаматтрансаминазы, обнаруженный А. Е. Браунштейном и С. М. Бычковым, объясняет, каким путем может происходить дезаминирование природных аминокислот в тканях, несмотря на слабую активность оксидаз аминокислот, катализирующих реакцию прямого дезаминирования этих аминокислот. [42]
Прибор состоит из реакционной ячейки и хроматографа. Реакцию дезаминирования осуществляют действием смеси NaNO3 и ледяной CH. [43]
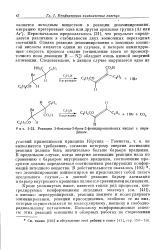 |
Реакция З - бензоил - З - бром-2 - фенилпропионовых кислот с пиридином. [44] |
Первоначально предполагалось [21], что результат определяется различием в стабильности двух возможных переходных состояний. Однако реакция дезаминирования с помощью азотистой кислоты является одним из случаев, в котором лимитирующая скорость процесса стадия ( отщепление азота от промежуточного иона диазония R - N. [45]
Страницы: 1 2 3 4