Значение - стандартный электродный потенциал
Cтраница 3
В табл. 4.1 представлены значения стандартных электродных потенциалов по отношению к СВЭ для некоторых электрохимических полуреакций восстановления в водных растворах. Данные приведены по убыванию отрицательного потенциала, чему отвечает снижение восстановительной и рост окислительной активности. [31]
 |
Стандартные электродные потенциалы металлов. [32] |
В таблице 18 представлены значения стандартных электродных потенциалов некоторых металлов. Символом Ме / Ме обозначен металл Me, погруженный в раствор его соли. Стандартные потенциалы электродов, выступающих как восстановители по отношению к водороду, имеют знак -, а знаком отмечены стандартные потенциалы электродов, являющихся окислителями. [33]
В таблицах обычно приводят значения стандартных электродных потенциалов. Па практике электрохимические процессы проподят в условиях, отличающихся ог стандартных. Реальные равновесные электродные потенциалы зависят от концентрации, температуры, состава электролита и могут зависеть в некоторых случаях от кислотности среды. Учет всех факторов, определяющих напряжение, необходимое для протекания электролиза, требует знания многих величин. Обычно значение этого напряжения сначала лишь оценивается, а точно устанавливается экспериментальным путем. [34]
 |
Насыщенный каломельный электрод сравнения. [35] |
В табл. 3 приведены значения стандартных электродных потенциалов металлов в водных растворах при 25 С. Величина равновесного электродного потенциала зависит от природы металла и растворителя, температуры и активности ионов металла в электролите. [36]
 |
Насыщенный каломельный электрод сравнения. [37] |
В табл. 3 приведены значения стандартных электродных потенциалов металлов в водных растворах при 25 С. Величина равновесного электродн) потенциала зависит от природы металла и растворителя, т пературы и активности ионов металла в электролите. [38]
Почему так сильно отличаются значения стандартных электродных потенциалов меди и цинка, хотя в таблице периодической системы элементы Си и Zn расположены рядом. [39]
Этот критерий позволяет по значениям стандартных электродных потенциалов предсказать возможность или невозможность разделения любой заданной пары ионов. [40]
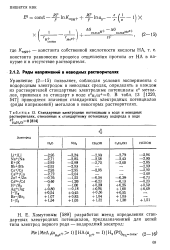 |
Стандартные электродные потенциалы в воде и неводных растворителях, отнесенные к стандартному потенциалу водорода в воде. [41] |
В табл. 13 [1220, 547] приводятся значения стандартных электродных потенциалов ( ряды напряжений) металлов в некоторых растворителях. [42]
 |
Влияние растворителей на стандартные электродные потенциалы при 25 С ( в В. [43] |
Его работы показали, что значения стандартных электродных потенциалов различных систем сильно зависят от природы растворителя. [44]
До какой предельной величины согласно значениям стандартных электродных потенциалов может дойти efe концентрация в ванне по отношению к концентрации ионов меди. [45]
Страницы: 1 2 3 4