Ферментативная реакция
Cтраница 1
Ферментативная реакция должна проводиться в строго определенных условиях с учетом следующих факторов. [1]
Ферментативные реакции 334, 335 Феррофосфор, утилизация 454 Фика закон 122 Фильтрование 206 ел. [2]
Ферментативные реакции часто исследуют, присоединяя к молекулам субстрата фрагмент, поглощающий свет ( хромофор), атомная конфигурация которого остается неизменной в течение реакции, хотя его энергетические уровни меняются. Электронные изменения обнаруживают, изучая поглощение системы как функцию времени. Приведенный рисунок показывает изменение поглощения такого хромофора в ходе реакции, катализируемой трипсином при величине рН 5 3 и температуре 25 С; длина волны 470 нм. [3]
Ферментативные реакции протекают часто с участием двух-трех субстратов и с образованием нескольких продуктов. Промежуточные продукты не могут накапливаться безгранично - либо они выводятся из организма, либо он гибнет. [4]
Ферментативные реакции представляют собой обычные термически активируемые процессы, протекающие с участием возбужденных колебательных и вращательных состояний молекул или структур активного центра. [5]
Ферментативные реакции, так же как и поверхностные, часто на всем своем протяжении или частично проявляют кинетику, известную как кинетика реакции нулевого порядка. [6]
Ферментативные реакции идут очень быстро, и их изучают методами, рассматриваемыми в гл. Кинетическое исследование этих систем осложняется трудностью получения чистых ферментов. Кроме того, механизмы реакций чрезвычайно сложны. [7]
Ферментативная реакция протекает в три стадии: 1) образование фермент-субстратного комплекса: Е 5 - ES - быстрая стадия, соответствующая фиксации субстрата на якорном участке активного центра. Ускорение реакции достигается за счет сближения и правильной ориентации субстратов относительно друг друга и увеличения их эффективной концентрации ( поскольку в растворе их столкновения случайны); 2) происходит химическая реакция через переходное состояние с образованием продукта реакции на поверхности фермента: ES - ъ EZ - ЕР. [8]
Ферментативные реакции, приводящие к утилизации глюкозы - фосфорилирование и окисление ее, а также образование гликогена протекают внутри клетки. Способствуя транспорту глюкозы внутрь клетки, инсулин тем самым обеспечивает ее утилизацию. Вместе с тем он не оказывает влияния на утилизацию углеводов бесклеточными гомоге-натами тканей ( гомогенаты получают путем растирания клеток, при котором разрушаются клеточные мембраны), так как механизм влияния инсулина на углеводный обмен связан именно с действием его на проницаемость клеточной мембраны. [9]
Ферментативная реакция проводится при температуре 30 С и рН среды: 4 7 - для грибных препаратов, 6 0 - для бактериальных и 4 8 - 4 9 - для солодовых. [10]
Ферментативные реакции частично подчиняются закону действующих масс, следовательно, их скорости зависят от концентрации фермента, субстрата и температуры. На скорость ферментативной реакции влияет также концентрация коферментов, активаторов и ингибиторов той или иной ферментативной реакции. [11]
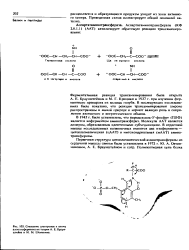 |
Смешение электронов к атому азота кофермента по теории А. Е. Браун-штейна и М. М. Шемякина. [12] |
Ферментативная реакция трансами ни ровання была открыта А. Е. Браунштейном и М. Г. Крицман в 1937 г. при изучении ферментного препарата из мышцы голубя. В последующих исследованиях было показано, что реакции трансаминнрования широко распространены в живой природе и играют важную роль в сопряжении азотистого и энергетического обмена. [13]
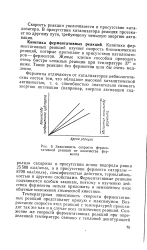 |
Зависимость скорости ферментативной реакции от количества фермента. [14] |
Ферментативные реакции подчиняются особым законам, поэтому к изучению действия ферментов нельзя приложить в неизменном виде обычные положения химической кинетики. [15]
Страницы: 1 2 3 4