Ферментативная реакция
Cтраница 2
Ферментативные реакции почти всегда тормозятся продуктами реакции. [16]
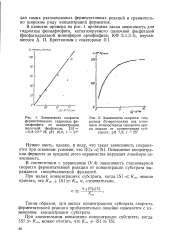
Ферментативные реакции часто исследуют, присоединяя к молекулам субстрата фрагмент, поглощающий свет ( хромофор), атомная конфигурация которого остается неизменной в течение реакции, хотя его энергетические уровни меняются. Электронные изменения обнаруживают, изучая поглощение системы как функцию времени. Приведенный рисунок показывает изменение поглощения такого хромофора в ходе реакции катализируемой трипсином при величине рН 5 3 и температуре 25 С; длина волны 470 им. [17]
Ферментативные реакции применялись еще в древности для производства вина, уксуса, пива и сыра. Их систематическое исследование было предпринято лишь в настоящее время. Старые наблюдения долгое время оставались вне какой-либо связи друг с другом. [18]
Ферментативные реакции, как будет показано далее, по своему механизму относятся именно к такого рода сложным процессам. [19]
Ферментативные реакции, в которых принимают участие более двух субстратов, встречаются очень редко. [20]
Ферментативные реакции, протекая через стадию образования комплекса ( переходного состояния), относятся к реакциям, протекающим по согласованному механизму. Согласованные реакции протекают в мягких условиях, неполярных растворителях и с очень высокими скоростями. [21]
Ферментативные реакции лучше всего идут при относительно невысокой ( около 40) температуре, а высокая температура ( как это будет изложено дальше) даже остановит реакцию. Реакции с помощью неорганического катализатора, наоборот, обычно ускоряются с повышением температуры. [22]
Ферментативные реакции, происходящие в процессе дыхания, в настоящее время хорошо изучены. [23]
Ферментативные реакции трансгликозилирования, при которых происходит перенос гликозильной группы на молекулы моно - или олиго-сахарида, являются основным путем биосинтеза олигосахаридов. [24]
Ферментативные реакции окисления - восстановления специально рассматриваются в части V, которая начинается с обсуждения ( гл. Белки типа ферредоксина участвуют в переносе электрона, они охарактеризованы в гл. [25]
Двухсторонние ферментативные реакции характеризуются замедлением процесса по мере образования продукта реакции, вследствие чего их кинетика ( зависимость концентрации субстрата от времени) даже в стационарной стадии выражается графически в форме кривой. Следует сказать, что задача нахождения начальной скорости реакции в ферментативной кинетике возникает часто. Дело в том, что замедление ферментативной реакции со временем наблюдается не только в случае двухсторонних реакций, но даже и при односторонних процессах. Причиной этого может быть, например, часто встречающееся торможение процесса продуктами реакции, весьма осложняющее кинетику прямой реакции и не всегда поддающееся кинетической интерпретации. В этих случаях вычисление начальной скорости реакции, когда концентрация ингибирующего продукта реакции близка к нулю, позволяет избежать ошибки в расчете кинетических констант. [26]
Ферментативные реакции клеток, в ходе которых химическая энергия извлекается из молекул питательных веществ и используется для синтеза и сборки компонентов клетки. [27]
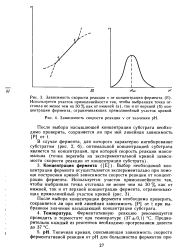
Оразных ферментативных реакций в сравнительно широком ряду концентраций ферментов. [29]
Страницы: 1 2 3 4