Катализируемая реакция
Cтраница 1
Катализируемые реакции можно проводить также таким образом, что в реакцию вводят определенное небольшое каталитическое количество катализатора С. В этом случае концентрация катализатора мала по сравнению с концентрацией субстрата S, так что при достаточно высоких концентрациях субстрата можно достигнуть насыщения катализатора. [1]
Катализируемые реакции в смысле теории Эйринга идут по пути сравнительно низкой свободной энергии активации по сравнению с той же самой реакцией, протекающей без катализатора. [2]
Катализируемые реакции характеризуются значительно более низкими энтальпиями активации, чем некатализируемые, но энтропии активации первых значительно ниже, чем у вторых. Оба этих эффекта компенсируют друг друга, так что свободные энергии активации обоих процессов мало отличаются друг от Друга. [4]
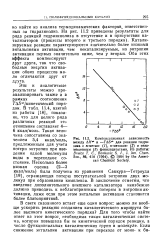
Катализируемой реакции; надстрочные индексы означают, что каталитическая реакция имеет первый или второй порядок относительно реагентов. Типичные результаты при использовании в качестве растворителя четыреххлористого углерода) приведены в табл. 21, в которой указаны катализаторы, величины & с и параметры активации Ас и Ес. Можно видеть, что в рассматриваемом случае каталитический эффект достигается главным образом снижением энергии активации, а не повышением энтропии активации. Реакция ( 63) не катализируется фенолами или основаниями. Ряд акцепторов протона [211] замедляет или подавляет кислотно-каталитический эффект в обеих реакциях. [5]
Скорость катализируемой реакции пропорциональна концентрации катализатора и несколько понижается с увеличением концентрации спирта, что может объясняться координированием спирта с катализатором. [6]
Скорость катализируемой реакции различна в зависимости от субстрата. [7]
Скорость катализируемой реакции пропорциональна концентрации катализатора и обычно очень легко определяется фотометрически путем измерения светопоглощения желтой окраски раствора в зависимости от времени. [8]
Скорость катализируемой реакции прямо пропорциональна подвижности активного протона. [9]
Скорость катализируемой реакции прямо пропорциональна подвижности активного протона. [10]
Для катализируемой реакции димеризации циклопентадиена уравнение ( 64) справедливо только в случае р-нафталин-сульфокислоты, а уравнение ( 65) применимо к другим кислотам. Это можно объяснить тем, что k & / № xc S 2 / - i где индекс а относится к кислотам примеров 13 - 17 табл. 21, а индекс р - к р-нафталинсульфокис-лоте. Кроме того, возможно, что 1i, или С - Последнее неравенство может быть следствием того, что анион В - ионной пары, участвующей в реакции ( 67), в случае 0-нафталинсульфокислоты имеет относительно больший объем. Предполагаемый механизм с переносом протона подтверждается наблюдаемой зависимостью между константой скорости каталитической реакции и константой диссоциации кислоты - катализатора, а также замедлением общей скорости при добавлении акцептора протона. [11]
Описаны также катализируемые реакции енового синтеза и го-модиепового синтеза, родственные катализируемой диеновой конденсации. [12]
Увеличение скорости катализируемой реакции связано либо с меньшей энергией активации нового пути реакции, либо с возможностью ее протекания по цепному механизму. [13]
В гетерогенном катализе катализируемая реакция происходит на поверхности раздела между твердым телом и газообразной или жидкой смесью реагентов. В гомогенном катализе реакция происходит либо в газовой смеси, либо в жидкости, где растворены как катализатор, так и реагенты. [14]
Коферменты определяют природу катализируемой реакции. [15]
Страницы: 1 2 3 4