Обратимая электрохимическая реакция
Cтраница 2
Нетрудно заметить, что в случае обратимой электрохимической реакции iYt не зависит от плотности задаваемого тока и в координатах iyt - - I выражение (XI.39) можно изобразить прямой линией, параллельной оси абсцисс. [16]
Полуширина пика на инверсионных ДИП при обратимых электрохимических реакциях от г0 не зависит. [17]
Авторы [186] отмечают, что поскольку при обратимой электрохимической реакции отношение силы тока пика на ДИП к силе предельного тока на НИП равно ( 0 - 1) / ( о 1) [ см. уравнения ( 38) и ( 91) ] и не зависит от толщины диффузионного слоя, то ток пика на ДИП должен зависеть от параметров опыта при работе с вращающимся дисковым электродом таким же образом, как и предельный ток на НИП. [18]
По форме вольтамперограммы Л - ной гармоники при обратимой электрохимической реакции аналогичны Af-ной производной от классической полярографической волны. Следовательно, на вольтамперограмме Ж - ной гармоники наблюдается N экстремумов. [19]
При реакциях типа ( в) первичный продукт обратимой электрохимической реакции после химической реакции становится электрохимически неактивным веществом. [20]
Если на поверхности электрода, находящегося в растворе электролита-протекает обратимая электрохимическая реакция, то между электродом и раствором существует равновесный скачок потенциала, величина которого определяется активностями реагирующих частиц. [21]
 |
Вольтамперограмма переменного тока 10 - 5 М раствора Cd11, Ni11 и Zn на фоне 1 М МН4С1 1Л1 NH4OH. [22] |
При анализе методом ВПТ, как правило, стремятся использовать обратимые электрохимические реакции. [23]
Электрические аккумуляторы - это гальванические элементы, которые на основе обратимых электрохимических реакций могут многократно накапливать электрическую энергию и отдавать ее для потребления. [24]
Уравнение (XI.38) представляет собой зависимость потенциала от времени для случая обратимой электрохимической реакции. [25]
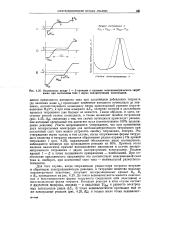 |
Взаимосвязь между / - Е - кривыми и кривыми потенциометрического титро вания при постоянном токе с двумя поляризуемыми электродами. [26] |
Для того случая, когда сопряженная редокс-пара титранта вступает в обратимую электрохимическую реакцию, а титруемое вещество вольтам-перометрически неактивно, получают поляризационные кривые Blt В2 и В3, приведенные на рис. 4.25. До точки эквивалентности имеются окисленная и восстановленная формы титруемого соединения ( обе неактивны) и восстановленная форма титранта. [27]
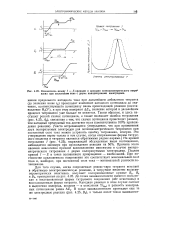 |
Взаимосвязь между / - - кривыми и кривыми потенциометрического титрош вания при постоянном токе с двумя поляризуемыми электродами. [28] |
Для того случая, когда сопряженная редокс-пара титранта вступает в обратимую электрохимическую реакцию, а титруемое вещество вольтам-перометрически неактивно, получают поляризационные кривые Въ В2 и В3, приведенные на рис. 4.25. До точки эквивалентности имеются окисленная и восстановленная формы титруемого соединения ( обе неактивны) и восстановленная форма титранта. Катодная реакция в этом случае состоит в выделении водорода, анодная - в окислении TrRed и разность электродных потенциалов равна A. [29]
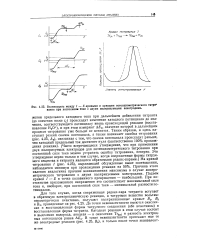 |
Взаимосвязь между / - . - кривыми и кривыми потенциометрического титро вания при постоянном токе с двумя поляризуемыми электродами. [30] |
Страницы: 1 2 3 4