Обратимая электрохимическая реакция
Cтраница 4
В статьях М. Г. Гуревича и соавторов рассмотрены пористые электроды, работающие в режиме принудительной подачи жидкости для случая обратимой электрохимической реакции. Далее принимается, что при плотности тока i коэффициент использования реагента в t / 1 пред - Оптимальное соотношение между входящей концентрацией реагента и скоростью его подачи в электрод зависит от параметров системы, а также от нагрузки на электрод. [46]
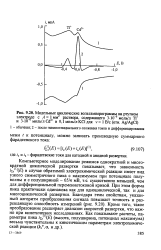 |
Модельные циклические вольтамперограммы на ртутном электроде с А 1 мм раствора, содержащего 3 - Ю 6 моль / л Т1 и 3 - КГ6 моль / л СсГ в ОД моль / л КС1 для v 1 В / с ( отн. Ag / AgCl. [47] |
Компьютерное моделирование режимов однократной и многократной циклической развертки показывает, что зависимость W ( Е) в случае обратимой электрохимической реакции имеет вид узкого симметричного пика с максимумом при потенциале полуволны и с полушириной - 65 / п мВ, т.е. существенно меньшей, чем для дифференциальной переменнотоковой кривой. При этом форма пика практически одинакова как для одноциклической, так и для многоциклической развертки. Кроме того, такое преобразование расширяет диапазон скоростей развертки, что важно при кинетических исследованиях. Как показывают расчеты, параметры пика / ь0) ( Е) ( высота, полуширина, потенциал максимума) весьма чувствительны к кинетическим параметрам электрохимической реакции ( ks a. [48]
Керн [698] показал, что по схеме ( XXIV) протекает анодное окисление аскорбиновой кислоты: в результате обратимой электрохимической реакции образуется неустойчивый промежуточный продукт, химически превращающийся в дегидроаскорбино-вую кислоту. Форма волны окисления аскорбиновой кислоты хорошо описывается теоретически выведенным уравнением, и ее ЕЧ, изменяется с периодом капания электрода так, как это предсказывает теория. [49]
Выражения (8.86) - (8.92) описывают зависимость i [ E ( t) ] в случае линейной диффузии и обратимой электрохимической реакции. При этом зависимость E ( t) задается, a i ( t) - измеряется, т.е. E ( f) является воздействием, а / ( О - отклик на это воздействие. Именно такой режим измерения предусмотрен практически во всех вольтамперометрических методах. [50]
Большой интерес представляет изученное Л. С. Загайновой и А. Г. Стромбергом [393] совместное действие двух поверхностно-активных веществ - камфоры и желатины - на обратимую электрохимическую реакцию, протекающую на амальгамном кадмиевом электроде в растворе соли кадмия. Желатина вплоть до концентрации 0 1 % не влияет на скорость электродного процесса, камфора оказывает сильное подавляющее действие. Добавление же желатины в раствор, насыщенный камфорой, снижает тормозящее действие камфоры, а при достаточной концентрации желатины - полностью устраняет его. Авторы [393] объясняют этот эффект изменением строения двойного слоя в присутствии желатины, способствующим ускорению электрохимической реакции. Однако можно предположить, что желатина, которая сама не тормозит указанного процесса, вытесняет с поверхности электрода камфору и тем самым устраняет обусловленное камфорой тормозящее действие. [51]
Большой интерес представляет изученное Л. С. Загайновой и А. Г. Стромбергом [393] совместное действие двух поверхностно-активных веществ - камфоры и желатины - на обратимую электрохимическую реакцию, протекающую на амальгамном кадмиевом электроде в растворе соли кадмия. Желатина вплоть до концентрации 0 1 % не влияет на скорость электродного процесса, камфора оказывает сильное подавляющее действие. Добавление же желатины в раствор, насыщенный камфорой, снижает тормозящее действие камфоры, а при достаточной концентрации желатины - полностью устраняет его. Авторы [393] объясняют этот эффект изменением строения двойного слоя в присутствии желатины, способствующим ускорению электрохимической реакции. Однако можно предположить, что желатина, которая сама не тормозит указанного процесса, вытесняет с поверхности электрода камфору и тем самым устраняет обусловленное камфорой тормозящее действие. [52]
В качестве электрода ( полуэлемента) сравнения могут служить такие электроды, на поверхности которых при соприкосновении с подходящим раствором возникают лишь обратимые электрохимические реакции. Благодаря этому приобретаемые ими с большой скоростью потенциалы устойчивы. При прохождении небольших токов в замкнутой цепи потенциалы таких полуэлементов практически остаются постоянными, поэтому их причисляют к неполяризуемым электродам. [53]
Регистрируемая вольт-амперная зависимость фарадеевского тока, как и в случае РКЭ, характеризует в основном импульсную составляющую и имеет форму пика с максимумом при п 0 в случае обратимой электрохимической реакции. При этом искажения пика за счет постоянното-ковой составляющей невелики. [54]
По нашему мнению [3], для обеспечения стабильности электрических потенциалов ИСЭ с твердым контактом необходимо, чтобы переход от ионной проводимости в мембране к электронной в токоотводе осуществлялся за счет обратимой электрохимической реакции. Нами [3] описаны электроды с твердым контактом, селективные к хлоридным, бро-мидным и тиоцианатным ионам, отличающиеся высокой стабильностью потенциалов во времени. [55]
Сравнение выражений (XI.37) и (XI.40) показывает, что в противоположность реакции, контролируемой стадией, разряда, прямые р - lg ( l T - t) для разных плотностей тока при обратимой электрохимической реакции не совпадают, а отстоят одна от другой на расстоянии, определяемом величиной задаваемой плотности тока i. [56]
Временной способ селекции основан на том, что при скачкообразном изменении электродного потенциала емкостный ток уменьшается существенно быстрее фарадеевского: первый уменьшается по экспоненциальному закону, а второй - по закону INt для обратимой электрохимической реакции и еще медленнее - для необратимой реакции. [57]
S 5 мВ) при одних и тех же значениях ta, ta, E0 и инструментальной чувствительности прибора ( в случае необходимости высоту волны и высоту пика пересчитывают на одну и ту же инструментальную чувствительность) для заведомо обратимых электрохимических реакций с тем же значением п, что и у исследуемой квазиобратимой реакции. [58]
Незначительная величина сопротивления медного электрода в пассивном состоянии, измеренная при частоте переменного тока 10 000 щ, приводит к выводу о том, что в пассивном состоянии на медном электроде в щелочи, помимо медленной реакции окисления меди, протекает какая-то быстрая обратимая электрохимическая реакция. [59]
Для эффективной многократной регенерации элементов необходимо, чтобы цинковый стаканчик элемента не имел механических повреждений и отверстий, возникших в результате взаимодействия с электролитом; элемент не был разряжен до напряжения ниже 0 7 в и не был слишком высохшим, так как при недостатке электролита нельзя осуществить обратимую электрохимическую реакцию. Кроме того, было установлено, что всегда лучше регенерируются элементы с меньшим сроком хранения, а также элементы, разряжаемые большим током. [60]
Страницы: 1 2 3 4