Диметиламиногруппа
Cтраница 1
Диметиламиногруппа является весьма сильным донором электронов; по этой причине N, N-диметиланилин легко вступает в реакцию азосочетания в качестве азокомпоненты. Однако элект-ронодонорное влияние этой группы на бензольное ядро проявляется в полной мере только в том случае, когда р-орбитали диметил-аминогруппы параллельны л-орбиталям ароматического ядра. В М Н 2 6 - тет1раметиланилине Диметиламиногруппа из-за пространственных затруднений выведена из плоскости, в которой она может в достаточной степени влиять на связанное с ней бензольное ядро. Последнее поэтому теряет свою активность в реакции азосочетания. [1]
Диметиламиногруппа ориентирует в орто - и пара-положения. [2]
Диметиламиногруппа ориентирует в орто - и пара-положения. Почему при нитровании диметиланилина в концентрированной серной кислоте образуется главным образом л-нитро-диметиланилин. [3]
Диметиламиногруппа при С4 расположена в а-положени и к кетон-ному карбонилу и вследствие этого обладает значительной подвижностью. Реакция является обратимой и, очевидно, протекает через цвиттерионную форму аминоенолов ( 1 7); механизм этой изомеризации не вполне ясен, и предложенные для его объяснения схемы ( см., например 470) носят гипотетический характер. Другой типичной особенностью диметиламиногруппы тетрациклинов является ее способность к восстановительному отщеплению. Эта реакция, приводящая к 4-дедиметиламинотетрациклинам ( 9), легко протекает при непродолжительном восстановлении Zn в АсОН либо самих тетрациклинов ( 1), либо ( что лучше) их четвертичных солей. [4]
Диметиламиногруппа, наряду с большим батофлорным эффектом, увеличивает интенсивность свечения примерно в два раза. [5]
Диметиламиногруппа проявляет сильный М - эффект по отношению к карбонильному атому углерода, а га-метильная группа соответственно / - эффект. [6]
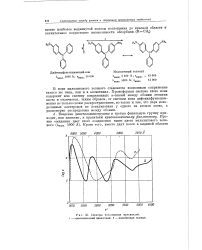 |
Спектры поглощения красителей. 1 - кристаллический фиолетовый. 2 - малахитовый зеленый. [7] |
Введение диметиламиногруппы в третью фенильную группу приводит, как известно, к красителю кристаллическому фиолетовому. [8]
Замена диметиламиногруппы на фосфазогруппу в гемицианинах XVI - XIX ( табл. 2) вызывает батохромный сдвиг порядка 20 ммк. [9]
Наличие диметиламиногруппы ( V) вызывает возникновение нового очень интенсивного длинноволнового максимума в области 440 нм. Максимум в области 330 нм малоинтенсивен и в ряде случаев перекрыт новой длинноволновой полосой. Вообще, кольцо б настолько чувствительно к изменению донорноакцепторных свойств заместителя, что даже замена диметиламиногруппы на диэтиламиногруппу ( соединения V и VI; IX и X) вызывает заметный сдвиг длинноволнового максимума. [10]
Так как диметиламиногруппа является уже сильным ауксо-хромом, то соединения, содержащие ее, находят большое применение в качестве аналитических реактивов. [11]
Например, диметиламиногруппа обладает ( А / - эффектом), т.е. способностью смещать неподеленные пары р-электронов по направлению к связанной к ней сопряженной системе, например, бензольному кольцу; нитрогруппа имеет ( - М эффект), т.е. притягивает я - электронную плотность. [12]
Эффект сопряжения диметиламиногруппы больше эффекта сопряжения аминогруппы, поскольку замена атомов водорода на ме-тильные группы увеличивает электронную плотность на атоме азота. [13]
Амино - или диметиламиногруппы являются донорными вследствие отталкивающего эффекта неподеленных пар электронов азота. Если из-за пространственных помех уменьшается сопряжение, можно предполагать, что отталкивание электронов неподеленных пар тоже будет оказывать меньшее действие на остаток молекулы и индуктивный эффект аминогруппы уменьшится. [14]
В конфигурации XII диметиламиногруппа, вероятно, почти плоская, однако она находится в плоскости, перпендикулярной к плоскости бензольного кольца. [15]
Страницы: 1 2 3 4