Рост - теплота - адсорбция
Cтраница 1
 |
Теплоты адсорбции NH3 ( a и СОц ( б на цеолитах типа L. [1] |
Рост теплот адсорбции в области Небольших заполнений и рост деформаций электронной структуры молекул с уменьшением размера катиона в ряду щелочных металлов ( наблюдаемый обычно при использовании спектральных методов) является весьма распространенной, но не общей закономерностью при адсорбции молекул, способных к специфическим взаимодействиям с катионами. Особенности структуры цеолита, возможность заселения катионами экранированных позиций в решетке, различия в степени экранирования катионов разных размеров электростатическим полем атомов кислорода, миграция катионов в процессе адсорбции и, наконец, природа адсорбата-все эти факторы определяют многообразие вариантов изменений в системах цеолит-ад-сорбат с изменением размеров и концентрации катионов. [2]
Рост теплоты адсорбции Н2О на цеолите ( K Na) - X, начинающийся после минимума на кривой примерно при 90 молек. При этом образуются левые энергетически более выгодные структуры ( кольца или цепи) из молекул воды, связанных между собой водородными связями, и при заполнениях около 150 молек. [3]
 |
Теплоты адсорбции органических паров углем. [4] |
Замещение водородных атомов атомами хлора в СН вызывает рост теплоты адсорбции. Замещение первого атома приводит к наибольшему росту; каждая последующая замена вызывает меньший рост. [5]
 |
Теплоты адсорбции органических паров углем. [6] |
Замещение водородных атомов атомами хлора в СН4 вызывает рост теплоты адсорбции. Замещение первого атома приводит к наибольшему росту; каждая последующая замена вызывает меньший рост. [7]
Можно сформулировать следующую закономерность: реакционная способность хемосорбированных молекул с ростом теплоты адсорбции падает до определенной точки, соответствующей элементу, расположенному недалеко от конца ряда переходных металлов. [8]
Существуют и другие причины, помимо узких промежутков пор, которые обусловливают рост теплот адсорбции. Атомы, находящиеся на ребрах и углах кристаллов, обладают различной степенью ненасыщенности по сравнению с теми, которые находятся: - на гладкой поверхности, поэтому их энергия взаимодействия с молекулами газа будет различной. [9]
Существуют и другие причины, помимо узких промежутков пор, которые обусловливают рост теплот адсорбции. Атомы, находящиеся на ребрах и углах кристаллов, обладают различной степенью ненасыщенности по сравнению с теми, которые находятся - на гладкой поверхности, поэтому их энергия взаимодействия с молекулами газа будет различной. [10]
Поскольку вклад ион-квад-рупольных взаимодействий при адсорбции Н2 и О2 должен быть невелик, рост теплот адсорбции для этих молекул обусловлен, как. [11]
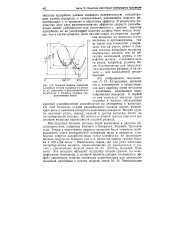 |
Влияние энергии ( теплоты адсорбции атомов водорода на металле на изменение термодинамического потенциала в процессе разряда гид-роксониевых ионов. [12] |
В результате наложения этих двух противоположных эффектов скорость рекомбинации может уменьшаться или увеличиваться с ростом теплоты адсорбции, но ее ускоряющее влияние должно быть всегда меньше, чем в случае разряда. Хотя данные опыта по теплотам адсорбции водорода на металлах малочисленны и противоречивы, тем не менее они позволяют утверждать, что на ртути, цинке и кадмии теплоты адсорбции водорода значительно меньше, чем на металлах платиновой группы и семейства железа. Следовательно, на ртути, например, условия более благоприятны для замедленного протекания разряда, а на никеле - для замедленной рекомбинации. [13]
 |
Изотермы адсорбции аргона на термической саже Sterling, 2700 9С ( называемой ранее Р-33 при 77 8 К. Температуры обработки образцов сажи и размеры кристаллов графита указаны у кривых. [14] |
Типичное для неоднородной поверхности уменьшение теплоты адсорбции с ростом заполнения поверхности исходной сажи сменяется ростом теплоты адсорбции на графитированной саже по мере заполнения первого адсорбционного слоя. В этом случае отчетливо проявляется переход от преимущественной адсорбции в первом слое адсорбированных молекул к преимущественной адсорбции во втором и последующих слоях. Этот переход вызывает резкое падение теплоты адсорбции после максимума и приближение ее к теплоте конденсации. [15]
Страницы: 1 2 3 4