Рост - теплота - адсорбция
Cтраница 2
 |
Влияние энергии ( теплоты адсорбции атомов водорода на металле на изменение термодинамического потенциала в процессе разряда гид-роксониевых ионов. [16] |
В результате наложения этих двух противоположных эффектов скорость рекомбинации может уменьшаться или увеличиваться с ростом теплоты адсорбции, но ее ускоряющее влияние должно быть всегда меньше, чем в случае разряда. Хотя данные опыта по теплотам адсорбции водорода на металлах малочисленны и противоречивы, тем не менее они позволяют утверждать, что на ртути, цинке и кадмии теплоты адсорбции водорода значительно меньше, чем на металлах платиновой группы и семейства железа. Следовательно, на ртути, например, условия более благоприятны для замедленного протекания разряда, а на никеле - для замедленной рекомбинации. [17]
Хорошо известно, что если ( Л) является определяющей скорость стадией, то энергия активации этой реакции уменьшается с ростом теплоты адсорбции атомов водорода на электроде. Подобное различие обусловлено тем, что в процессе ( В) фигурирует потенциальная энергия состояния перед переходным состоянием; в процессе ( А) выражение для потенциальной энергии характеризует состояние системы после переходного состояния. [18]
В 1928 г. А. Н. Фрумкин вывел уравнение для взаимодействия адсорбированных частиц. Взаимное притяжение приводит к росту теплоты адсорбции, отталкивание - к ее уменьшению. [19]
 |
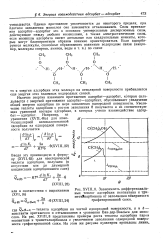
Зависимость дифференциальных теплот адсорбции неопентана и три-метилкарбинола от заполнения поверхности графитированной сажи. [20] |
На рис. XVIII, 8 представлены примеры роста теплоты адсорбции паров неопентана и триметилкарбинола с увеличением заполнения однородной поверхности графитированной сажи. [21]
 |
Зависимость дифференциальных теплот адсорбции неопентана и три-метийкарбинола от заполнения поверхности, графитированной сажи. [22] |
На рис. XVIII, 8 представлены примеры роста теплоты адсорбции паров неопентана и триметилкарбинола с увеличением заполнения однородной поверхности графитированной сажи. На этом же рисунке пунктиром проведены линии. [23]
На рис. XVIII, 8 представлены примеры роста теплоты адсорбции паров неопентана и триметилкарбинола с увеличением заполнения однородной поверхности графктированной сажи. [24]
Это в большой степени вызвано тем, что в предыдущей работе не было обращено должного внимания на возможность увлажнения сорбента во время эксперимента. Для образцов 2 - 4 с увеличением степени замещения катионов натрия на ион кальция характерен рост теплот адсорбции ненасыщенных соединений и окиси углерода, в то время как теплоты адсорбции предельных соединений практически мало изменяются. На калиевой форме цеолита значения теплот адсорбции предельных углеводородов по сравнению с натриевой формой цеолита мало изменяются; что касается величин теплот адсорбции ненасыщенных соединений, то они уменьшаются. [25]
Это объясняется тем, что различие мест по энергиям адсорбции внутри периодически повторяющегося участка в полости цеолита по отношению к молекулам группы А, неспособным к специфической адсорбции, гораздо меньше, чем по отношению к молекулам группы В. В случае ксенона это небольшое различие мест внутри полости цеолита HLiNaX не подавляет проявления межмолекулярного притяжения адсорбат - адсорбат, вызывающего рост теплоты адсорбции. [26]
Как видно из рис. 11.23, для цеолита Са - Е вплоть до заполнений около 1 молекулы СО2 на катион Са24 - характерны существенно более высокие теплоты адсорбции, чем для цеолита Na-E. В то же время для цеолитов X, Y и А замещение Na на Са2 - 1 - приводит к росту теплоты адсорбции лишь в области малых заполнений. [27]
Он показал, что теплоты адсорбции водорода и этилена уменьшаются по мере возрастания веса с. Бик объяснил это тем, что связь возникает за счет имеющихся в rf - зоне незанятых орбит, количество которых по мере увеличения веса cf - состояний для металлической связи будет уменьшаться. С ростом теплот адсорбции водорода и этилена происходит снижение скорости гидрогенизации. [28]
Для всех веществ ( кроме пропилена) обнаружено значительное отклонение шостер от линейности в области низких температур. Изменение наклона изостер ( иногда в довольно широком интервале температур) рассматривается как указание на изменение состояния адсорбируемых молекул. Степень искривления изостер растет с ростом теплоты адсорбции. Очень большие изменения наклона изостер не позволяют интерпретировать этот излом как фазовый переход типа плавления и заставляют рассматривать его как постепенный переход одного состояния адсорбированных молекул в другое состояние ( переход типа локализация-делокализация), связанный с изменением взаимодействий адсорбат-адсорбент. [29]
Страницы: 1 2 3 4
