Рост - теплота - адсорбция
Cтраница 3
Это показывает, что молекулы нормальных углеводородов ориентируются на поверхности плоско. Влияние молекулярного веса на энергию адсорбции особенно заметно у низших углеводородов, у которых относительное увеличение молекулярного веса при переходе к следующему члену гомологического ряда больше. Такое расположение молекул н-алка-пов и свяганный с ними рост теплоты адсорбции на каждую группу СШ на постоянный для данного адсорбента инкремент характерен и для других адсорбентов. [31]
Интересно отметить подтвержденную на опыте зависимость тока обмена [ 4, И ] реакции выделения водорода от теплоты адсорбции водорода [12] на металле. В кислых растворах для Pd, Rh, An, Ni, Fe, Cu, ( а, Mo, W и Та найдено, что ] g i0 закономерно уменьшается с ростом АНн. Для Hg, T1, РЬ и Sn наблюдается менее ясно выраженная взаимосвязь этих величин. Поэтому на значительном число металлов ток обмена действительно уменьшается с ростом теплоты адсорбции, так что для этих металлов реакция ( В) определяет скорость процесса. [32]
Так, было предположено, что при увеличении теплоты адсорбции водородных атомов на катодном металле вероятность замедленного разряда падает, а замедленной рекомбинации растет. Это связано с различным влиянием изменения теплоты адсорбции водородных атомов на скорость разряда и на скорость рекомбинации. Как следует из потенциальных кривых ( рис. 19.5), энергия активации разряда уменьшается с ростом теплоты адсорбции. Энергия активации процесса рекомбинации, напротив, увеличивается с упрочнением связи между металлом и поверхностными атомами водорода, количественной характеристикой которой является теплота адсорбции. [33]
Было предположено, что при увеличении теплоты адсорбции водородных атомов на катодном металле вероятность замедленного разряда падает, а вероятность замедленной рекомбинации растет. Это связано с фактом различного влияния изменения теплоты адсорбции водородных атомов на скорость разряда и рекомбинации. Как следует из потенциальных кривых ( см. рис. 70), энергия активации разряда уменьшается с ростом теплоты адсорбции. Энергия активации процесса рекомбинации, напротив, увеличивается с упрочнением связи между металлом и поверхностными атомами водорода, количественной характеристикой которой является теплота адсорбции. В результате наложения этих двух противоположных эффектов скорость рекомбинации может уменьшаться или увеличиваться с ростом теплоты адсорбции, но ускоряющее влияние должно быть всегда меньше, чем в случае разряда. Хотя число данных по теплотам адсорбции водорода на металлах ограничено и они противоречивы, тем не менее можно утверждать, что на ртути, цинке и кадмии теплоты адсорбции водорода значительно меньше, чем на металлах платиновой и железной групп. Так, например, на ртути условия более благоприятны для замедленного протекания разряда, а на никеле - для замедленной рекомбинации. Эти соображения, высказанные автором в 1949 г. привели его к заключению о существовании двух крайних групп металлов с различным механизмом перенапряжения водорода. К первой из них относятся металлы платиновой и железной групп, обладающие высокой адсорбционной способностью по отношению к водороду. На этих металлах стадия рекомбинации должна играть решающую роль в кинетике катодного выделения водорода. Вторая группа включает ртуть, свинец, кадмий и другие металлы, почти не адсорбирующие водород. На металлах второй группы кинетика выделения водорода определяется стадией разряда. Впоследствии подобные же взгляды были высказаны и другими исследователями, например Коквеем к Бокрисом. [34]
Так, было предположено, что при увеличен-ии теплоты адсорбции водородных атомов на катодном металле вероятность замедленного разряда падает, а замедленной рекомбинации растет. Это связано с различным влиянием изменения теплоты адсорбции водородных атомов на скорость разряда и на скорость рекомбинации. Как следует из потенциальных кривых ( см. рис. 79), энергия активации разряда уменьшается с ростом теплоты адсорбции. Энергия активации процесса рекомбинации, напротив, увеличивается с упрочнением связи между металлом и поверхностными атомами водорода, количественной характеристикой которой является теплота адсорбции. В результате наложения этих двух противоположных эффектов скорость рекомбинации может уменьшаться или увеличиваться с ростом теплоты адсорбции, но ее ускоряющее влияние должно быть всегда меньше, чем в случае разряда. Следовательно, на ртути, например, условия более благоприятны для замедленного протекания разряда, а на никеле - для замедленной рекомбинации. Эти соображения, высказанные Антроповым в 1949 г., привели его к заключению о существовании двух крайних групп металлов с различным механизмом перенапряжения водорода. К первой из них относятся металлы платиновой и железной групп, обладающие высокой адсорбционной способностью по отношению к водороду. На этих металлах стадия рекомбинации должна играть решающую роль в кинетике катодного выделения водорода. Вторая группа включает ртуть, свинец, кадмий и другие металлы, почти не адсорбирующие водород. [35]
При значении адсорбции около 85 % от адсорбции при насыщении хъ теплота адсорбции имеет минимум, затем она начинает возрастать с ростом адсорбированного количества. Так как кривые сродства идут приблизительно параллельно друг другу, то ( дх / дТ) х практически постоянно, и хотя sx продолжает уменьшаться, этот процесс перевешивается внезапным ростом ( дгх / дх) р - наклона кривой сродства. Конечно, это является чисто формальным объяснением минимума теплоты адсорбции. Гольдман и Поляни не дали никакого физического объяснения, но, невидимому, является вероятным, что рост теплоты адсорбции при этих больших величинах адсорбции обязан появлению теплоты капиллярной конденсации. [36]
При значении адсорбции около 85 % от адсорбции при насыщении хъ теплота адсорбции имеет минимум, затем она начинает возрастать с ростом адсорбированного количества. Так как кривые сродства идут приблизительно параллельно друг другу, то ( dx / dT) v практически постоянно, и хотя ех продолжает уменьшаться, этот процесс перевешивается внезапным ростом ( dix / dx) y - наклона кривой сродства. Конечно, ото является чисто формальным объяснением минимума теплоты адсорбции. Гольдман и Поляни не дали никакого физического объяснения, но, невидимому, является вероятным, что рост теплоты адсорбции при этих больших величинах адсорбции обязан появлению теплоты капиллярной конденсации. [37]
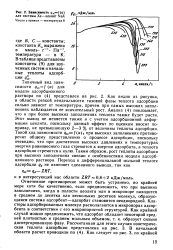 |
Зависимость. 5tf ( а для системы Хе цеолит NaX. [38] |
Как видно из рисунка, в области резкой неидеальности газовой фазы теплота адсорбции сильно зависит от температуры, причем при самых высоких заполнениях наблюдается ее значительный рост. Анализ ( 4) показывает, что и при более высоких заполнениях теплота также будет расти. Этот вывод не меняется также и с учетом адсорбционной деформации цеолита, поскольку данный эффект по оценкам вносит поправку, не превышающую 2 - 3 % от величины теплоты адсорбции. Такой ход зависимости gstf ( a) T ПРИ высоких заполнениях противоречит общему представлению о процессе адсорбции, поскольку очевидно, что при достаточно высоких давлениях и температурах энергия равновесного газа стремится к энергии адсорбата, а теплота адсорбции стремится к нулю. Таким образом, рост теплоты адсорбции при высоких заполнениях связан с особенностями модели адсорбционного раствора. [39]
Для ал-килбензолов с нормальной боковой цепью величины Qv определялись приблизительно в том же интервале температур, что и для соответствующих н-алканов. Теплота адсорбции при переходе от бензола к толуолу увеличивается на - 2 0 ккал / моль, а при переходе от толуола к этиленбензолу только на - 0 9 ккал / молъ. С дальнейшим ростом нормальной цепи у моноалкилбензолов рост теплоты адсорбции происходит практически так же, как у к-алканов, наклоны обеих прямых близки. [40]
Наличие на поверхности кремнезема таких примесей, как А1 и В, образующих сильные протонные и апротонные кислотные центры, вызывает увеличение энергии связи с электроподонорными молекулами. Это особенно сильно проявляется при дегидратации и дегидроксилировании поверхности, поскольку при этом обнажаются сильные апротонные кислотные центры. Дегидроксилирование поверхностей чистых кремнеземов снижает специфичность молекулярной адсорбции, уменьшая возможность образования водородной связи. Дегидроксилирование же кремнеземов, содержащих примеси А1 и В, приводит к сильному росту теплоты адсорбции молекул групп В и D. Этот эффект ярко проявляется на содержащих примеси А1 аэросилогелях после дегидроксилирования их поверхности при высоких температурах. Рост теплоты адсорбции связан с изменением именно химии поверхности, поскольку макропористые кремнеземы при этом практически не изменяют величину своей удельной поверхности и размеры пор и теплоты адсорбции молекул группы А не изменяются. [41]
Наличие на поверхности кремнезема таких примесей, как А1 и В, образующих сильные протонные и апротопные кислотные центры, вызывает увеличение энергии связи с электронодонорньтми молекулами. Это особенно сильно проявляется при дегидратации и дегидроксилировании поверхности, поскольку при этом обнажаются сильные апротонные кислотные центры. Дегидроксилирование поверхностей чистых кремнеземов снижает специфичность молекулярной адсорбции, уменьшая возможность образования водородной связи. Дегидроксилирование же кремнеземов, содержащих примеси А1 и В, приводит к сильному росту теплоты адсорбции молекул групп В и D. Этот эффект ярко проявляется на содержащих примеси А1 аэросилогелях после дегидроксилирования их поверхности при высоких температурах. Рост теплоты адсорбции связан с изменением именно химии поверхности, поскольку макропористые кремнеземы при этом практически не изменяют величину своей удельной поверхности и размеры пор и теплоты адсорбции молекул группы А не изменяются. [42]
Поэтому наклон этой линии при приведении величин QJ к одной температуре должен быть большим. Для ал-килбензолов с нормальной боковой цепью величины Ql определялись приблизительно в том же интервале температур, что и для соответствующих к-алканов. Теплота адсорбции при переходе от бензола к толуолу увеличивается на - - 2 0 ккал / молъ, а при переходе от толуола к этилепбензолу только на - - 0 9 ккал / молъ. С дальнейшим ростом нормальной цепи у моноалкилбензолов рост теплоты адсорбции происходит практически так же, как у к-алкапов, наклоны обеих прямых близки. [43]
Из рис. 1, па котором представлены изотермы н теплоты адсорбции аммиака, воды и метанола, видно, что заполнение каналов цеолита приблизительно на 20 о сопровождается наиболее значительным падением теплот адсорбции. Наиболее сильно продолжает снижаться кривая теплот для аммиака; в случае воды происходит ступенеобразное снижение кривой, а в случае метанола имеется небольшой максимум на кривой теплот адсорбции. Благодаря резкой специфичности адсорбции наличие метильной группы молекулы метанола не играет, при малых степенях заполнения, существенной роли. Возможно, что в случае воды имеется некоторое повышение теплоты адсорбции за счет проникновения молекул воды в малые полости; это, по-видимому, не может происходить ни в случае аммиака, ни в случае метанола. С увеличением адсорбции во всех случаях уменьшается эффективное расстояние между адсорбирующимися молекулами. В случае метанола сближение молекул ведет даже к росту теплоты адсорбции за счет взаимодействий адсорбат-адсорбат. Молекулы аммиака, взаимодействуя с ионами цеолита благодаря наличию одной свободной пары электронов, практически не имеют возможности связываться друг с другом в адсорбированном слое. Поэтому для аммиака характерно непрерывное падение теплот адсорбции по мере использования наиболее выгодных для адсорбции участков поверхности. Адсорбция пара воды занимает промежуточное ( по сравнению с метанолом и аммиаком) положение - молекулы воды даже при малых степенях заполнения выбирают на поверхности такие положения, которые позволяют им осуществлять весьма тесное взаимодействие между собой. [44]
Мы можем теперь вкратце суммировать выводы, приведенные в этом разделе. Часто наблюдаемое очень сложные формы кривых, показывающих изменение дифференциальных теплот адсорбции с количеством адсорбированного газа, могут быть, по крайней мере качественно, объяснены двумя факторами. Первым из них является неоднородность поверхности; атомы поверхности отделены различными расстояниями и расположены в различных геометрических конфигурациях, имеющих различные энергии взаимодействия с одной и той же молекулой; подобно этому, теплоты адсорбции в трещинах, щелях, впадинах, каналах и пустотах адсорбента отличны от теплот адсорбции на плоской поверхности. Вторым фактором является взаимодействие между адсорбированными молекулами: ориентационные силы приводят к отталкиванию, дисперсионные - к притяжению. Когда поверхность уже покрыта адсорбированным слоем, образование второго слоя вызывает изменение теплоты адсорбции. Обычно это изменение является уменьшением, но иногда находят при этом и рост теплоты адсорбции. [45]
Страницы: 1 2 3 4