Валентные связи
Cтраница 2
Если образуются две валентные связи, такого перехода электронов не происходит, поскольку, как следует из спектров, и у кислорода и у его гомологов основному состоянию атомов соответствует триплетный терм P i - Это значит, что атомы кислорода и его гомологов в основном состоянии содержат два неспаренных электрона. Следовательно, они могут проявлять валентность два, не требуя какой-либо энергии возбуждения, кроме энергии, необходимой для распада молекул на атомы, тогда как для проявления ими высших валентностей такая энергия возбуждения необходима. [16]
В атомных решетках валентные связи осуществляются парами электронов, движущихся по определенным орбитам, охватывающим оба связанных атома. [17]
В этиленовых углеводородах валентные связи деформированы, поэтому их модели собирают с помощью пружинных связей, хорошо иллюстрирующих напряженность. [18]
Получение препаратов, содержащих валентные связи между макромолекулами, может быть достигнуто и обработкой целлюлозы различными полифункциональными соединениями. [19]
На границе кристалла обрываются валентные связи, сильно искажается периодический потенциал, нарушается симметрия элементарных ячеек. Поэтому даже если кристалл ограничен идеальными плоскостями, расположение атомов на которых соответствует их расположению на эквивалентных плоскостях в глубине образца, зонная структура приповерхностного слоя будет отличаться от зонной структуры объема. [20]
При образовании резита многие валентные связи не могут быть осуществлены из-за пространственных условий и в макромолекулярном комплексе остаются свободные метилольные группы, которые можно рассматривать как неплотности, дырки в макромолекулярной решетке резпта ( стр. С другой стороны, значительные напряжения, которые создаются вследствие неравномерного и последовательного закрепления фенольных ядер, вызывают внутримолекулярные разрывы и образование микротрещин. [21]
С другой стороны, валентные связи возможны и в нек-рых соединениях тяжелых элементов, напр. [22]
При образовании резита многие валентные связи не могут быть осуществлены из-за пространственных условий и в макромолекулярном комплексе остаются свободные метилольные группы, которые можно рассматривать как неплотности, дырки в макромолекулярной решетке резита ( стр. С другой стороны, значительные напряжения, которые создаются вследствие неравномерного и последовательного закрепления фенольных ядер, вызывают внутримолекулярные разрывы и образование микротрещин. [23]
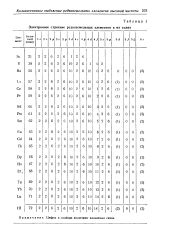 |
Электронное строение редкоземельных элементов в их солях. [24] |
Цифры в скобках включают валентные связи. [25]
 |
Молекулы Н20 ( а, СО2 ( б и С6Не ( в, окантованные ван-де. [26] |
Как уже отмечалось, валентные связи направленны и обладают свойством насыщения, поэтому объединяться в молекулу данного вещества может только определенное число атомов. При одном и том же атомном составе могут существовать молекулы разного строения, обладающие различными свойствами. Это явление называется изомерией. Различают структурную, поворотную и оптическую изомерии. [27]
Стрелками в формуле обозначены координационные валентные связи. [28]
 |
Структура плоскости ку-бической решетки.| Структура октаэдрической. [29] |
В следующем состоянии г уже валентные связи, а р и q либо равны О, либо слабые валентные связи. [30]
Страницы: 1 2 3 4