Валентные связи
Cтраница 3
Согласно теории Вант-Гоффа, валентные связи атома углерода направлены к вершинам правильного тетраэдра, в центре которого расположен углерод. [31]
На ней могут находиться свободные валентные связи атомов углерода, боковые цепи насыщенных и ненасыщенных углеводородов и соединения, содержащие кислород и серу. [32]
Для переходных металлов характерны делокализованные валентные связи с разными ненасыщенными системами, причем в образовании связи принимают участие полностью или частично заполненные cf - орбитали металла. [33]
Говоря о том, какие валентные связи образуются и разрываются в ходе некоторой заданной конкретной реакции, мы исходили из того, что этот вопрос однозначным образом интуитивно решается химиком, рассматривающим структурное уравнение реакции. Более правильным будет взгляд, согласно которому сведения об изменяющихся связях рассматриваются в качестве данных, устанавливаемых экспериментальным путем. Действительно, известны случаи, когда вопрос о том, какие валентные связи разрываются и образуются, выяснялся специальными экспериментами с применением меченых атомов. [34]
Поскольку переход электронов, образующих валентные связи, из устойчивого состояния в неустойчивое происходит за конечное время, существенную роль должны играть и кинетические эффекты. [35]
Одна черточка в формуле означает валентные связи атомов в молекуле каучука, две черточки означают двойные связи. Общая формула углеводородной цепочки натурального каучука ( CsHs), где п - количество изопентеновых групп ( звеньев) в молекуле. [36]
Исходя из того, что валентные связи тетраэдрического углеродного атома составляют угол, равный приблизительно 110, Байер в 1885 г. пришел к выводу, что в циклических соединениях существует напряжение, пропорциональное разности между этим углом и углом многоугольника, соответствующего циклу. [37]
Льюиса); - показывает все валентные связи ( с помощью черточек или точек) и соединяемые ими атомы. [38]
Четыре электрона каждого введенного атома образуют валентные связи с четырьмя соседними атомами кристаллической решетки, а пятый электрон остается свобод-ым. Такой избыточный электрон оказывается значительно слабее связанным со своим атомом Для того чтобы оторвать его от атома и превратить в свободный носитель зарядов, требуется значительно меньшее количество энергии, чем для высвобождения электрона из валентной связи. Уход электрона от атома введенного в германий вещества ( например, сурьмы) превращает этот атом в положительный ион. Этот положительный заряд будет прочно связан с кристаллической решеткой и не будет перемещаться подобно дырке. Таким образом, появление в кристаллической решетке германия примесного атома пятой группы приводит к появлению свободного электрона. Однако его существование не связано с одновременным существованием дырки. [39]
Электронные пары, осуществляющие координационную и валентные связи, различаются по своему происхождению. Так, электронная пара, ответственная за координационную связь, является парой р-электронов атома азота. Электронные же пары валентных связей образуются за счет спаривания неспаренных электронов атомов кислорода карбоксильных групп и электронов, находящихся на соответствующих орбиталях атома металла. [40]
Она гораздо менее прочна, чем валентные связи; для разрыва димера уксусной кислоты на две молекулы нужно затратить энергию около 14 ккал / молъ. Следовательно, энергия водородной связи составляет 7 ккал / молъ. Энергия же связи Н - Н в молекуле водорода составляет 108 4 ккал / молъ, тем не менее энергия водородной связи - заметная величина. [41]
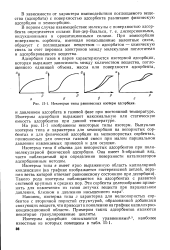 |
I. Некоторые типы равновесных изотерм адсорбции. [42] |
При хемосорбции поверхность сорбента, имеющая ненасыщенные валентные связи, образует с поглощаемым веществом - адсорбатом - химическую связь за счет переноса электронов между молекулами поглотителя и адсорбированного вещества. [43]
Мысль о том, что четыре валентные связи атома углерода направлены к углам правильного тетраэдра была высказана в 1874 г. голландским химиком Дж. [44]
При повышенной температуре под действием тепла валентные связи структурной сетки резины ослабевают и могут разрываться. [45]
Страницы: 1 2 3 4