Связывание - фермент
Cтраница 1
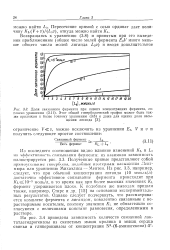
Связывание фермента с гидрофильной матрицей полимера заметно повыц его устойчивость к денатурации при нагревании. Полиакриламидные носит значительно инертнее целлюлоз, и поэтому физически адсорбирующиеся бе и ферменты легче отмываются от них, чем от целлюлозных носителей. Это; возможность значительно дольше повторно использовать полиакриламидные сители по сравнению с целлюлозными носителями. [1]
Связывание фермента, меченного флуоресцеином, на активированных бром-цианом сефарозе или сефадексе осуществляют аналогично связыванию немеченного фермента. Меченные флуоресцеином антитела связывают на ферменте, иммобилизованном на матрице, из 0 1 М раствора бикарбоната атрия. Неразбавленную меченую антисыворотку смешивают с равным объемом суспензии фермента, связанного с нерастворимым носителем, и термостатируют 1 ч при 37 С и еще 12 ч при 4 С. После перенесения материала на стеклянный фильтр неспецифически сорбированные компоненты удаляют интенсивным промыванием 0 1 М бикарбонатом натрия. [2]
Связывание фермента с субстратом, таким образом, является только одним ( хотя наиболее важным) из многих типов взаимодействий белок-лиганд, и мы, в первую очередь, кратко рассмотрим виды сил, участвующих в этих взаимодействиях. [3]
 |
Определение триптофансодер-жащего белка в присутствии коллагена. [4] |
После связывания ферментов с нерастворимыми носителями их свойства могут меняться либо под влиянием микроокружения, либо в результате изменений, вызванных химической модификацией благодаря образованию новых ковалентных связей. Следовательно, очень полезно охарактеризовать фермент не только определением общей ферментативной активности и количества связанного белка, но и путем титрования активных центров. [5]
Для связывания ферментов, антигенов и антител с нерастворимыми матрицами, как это указано в обзорах [78, 81], используется и ряд других носителей. Однако область их применения не столь широка. Например, производные полистирола [38, 40, 51, 59-61] больше не применяют, вероятно, из-за их гидрофоб-ности [16], делающей невозможным достаточно хороший контакт между водой и твердой фазой. [6]
 |
Строение гема и его связь с белком в цитохроме Р-450. [7] |
Тип связывания фермента с субстратом может быть установлен при помощи спектральных методов, поскольку связывание субстратов с цитохромом Р-450 изменяет его спектральные характеристики. Измерение спектра фермента в присутствии субстрата с использованием раствора фермента без субстрата в качестве контроля дает так называемый спектр различия. Субстраты, которые связываются с белковой частью цитохрома Р-450, имеют спектр различия при 390 нм. Такие субстраты называются субстратами первого типа. [8]
При связывании фермента на колонке при рН адсорбции 6 5 в верхней части ионообменника образуется ярко-красное кольцо мышечных белков, а по мере заполнения колонки белком целлюлоза приобретает опаловую, бледную желтизну. Граница раздела между матовой и желтовато-опаловой зонами постепенно продвигается книзу. После подачи на колонку буфера рН 7 9 ( КОН-трицин) красное кольцо мышечных белков начинает постепенно двигаться книзу, разделяясь при этом на несколько отдельных колец и прокрашивая целлюлозу в бледно-розовый цвет. После того как поглощение при 280 нм в элюате снизится до значения 0 1 - 0 2, на колонку подают буфер ( 10 мМ КОН-трицин, рН 7 9), содержащий вместо 3 мМ ацетата натрия 0 5 мМ 3-фосфоглицерат. [9]
В реакциях связывания фермента с субстратом ион металла часто нейтрализует отрицательные заряды анионных групп. [10]
Согласно Клотцу [48, 49], металл служит мостиком для связывания фермента с О, возникающим при присоединении ОН - к пептиду или амиду. [11]
 |
Бифуркационная диаграмма для системы. [12] |
Нелинейность подобной системы обусловлена торможением процесса в результате связывания фермента в неактивный комплекс ES2 при повышенных концентрациях субстрата; этот процесс аналогичен изменению свойств матрицы мембраны при значительной растворимости газов. [13]
Эта система служит интересной моделью, демонстрирующей, каким образом связывание фермента с субстратом может происходить значительно медленнее, чем со скоростью диффузии, хотя при этом не происходит образования новых или разрушения старых ковалентных связей. [14]
Страницы: 1 2 3 4