Дативная связь
Cтраница 1
 |
Схема образования связи в ацетиленовых комплексах нульвалентной платины. [1] |
Дативная связь осуществляется путем перекрывания заполненной гибридной ( dxz й 2) - орбитали металла с вакантной разрыхляющей пг ц - орбиталью ацетилена. Для эффективного перекрывания по типу дативной связи органический лиганд должен быть расположен в плоскости, перпендикулярной к остальной части молекулы. [2]
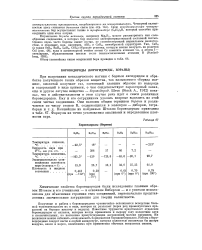
Дативная связь N-Si в 1-метил-силатране гораздо короче в кристалле [74], чем в газе [75], причем настолько, что, согласно данным, приведенным на рис. 9 - 63, вряд ли имеет смысл говорить о какой-либо связи в газовой фазе. Отсюда следует, что межмолекулярные силы в кристалле как бы сжимают молекулу вдоль координационной связи. Разумеется, часть этих различий газ-кристалл обусловлена различным физическим смыслом элект-ронографических и рентгеноструктурных параметров, поскольку образование подобных координационных связей сопровождается значительным переносом заряда. Можно полагать, что другая часть имеющихся различий носит действительно структурный характер, в чем убеждают изменения геометрических параметров в остальной части молекулы. [3]
Однако дативная связь, по-видимому, не имеет решающего значения, так как существуют вполне устойчивые соединения, например ( я - С5Н5) 2ТаН3, в которых атомы металла вовсе не имеют заполненных орбиталей; но когда металл имеет заполненную несвязывающую орбиталь, дативное взаимодействие упрочняет связь металла с кольцом. [4]
Образование дативной связи и перенос электронов на разрыхляющие орбитали оксида углерода приводит к увеличению электронной плотности на атоме кислорода и электрофильности атома углерода. [5]
Влияние дативной связи особенно важно при образовании я-комплекса по механизму вытеснения. Взаимодействие не занятых в связях d - электронов центрального атома с разрыхляющими орбиталями ненасыщенного соединения осуществляется на расстояниях, больших, чем те, которые необходимы для осуществления донорно-акцепторной связи. Дативное взаимодействие обеспечивает предварительную ориентацию реагентов и облегчает последующий процесс замещения. [6]
 |
Строение аниона соли Цензе. [7] |
Наличие дативной связи является важным условием устойчивости тс-комплексов. [8]
Прочность траясаннулярной дативной связи N: - Si зависит от электроноакцептор Ной способности второго аксиального заместителя. [9]
В образовании дативной связи в комплексах участвует неподеленная пара электронов кислорода. На рис. 6 - 10 показаны спектры ЭПР, наблюдаемые при комнатной температуре при адсорбции ДТБН на NH4Y, активированном при 300 и 500 С соответственно. Спектр на рис. 6 - 10, а характеризуется в основном тензором, описывающим анизотропное сверхтонкое взаимодействие ( А А О) с ядром 14N в поле аксиальной симметрии. Спектр соответствует структуре II, в которой неспаренный электрон находится на рп - орбитали азота, расположенной перпендикулярно плоскости молекулы. Он приписывается водороду ДТБН, связанному с HY. [10]
При этом возникает дативная связь и образуются соединения типа ВРз-МНз. Способность фосфора, серы и более тяжелых атомов проявлять высокие валентные состояния объясняется тем, что энергия, необходимая для перемещения, скажем, Зз-электро-нов в фосфоре на вакантную Зй-орбиталь, не настолько велика, чтобы препятствовать этому переходу. Химические и физические свойства атомов или ионов определяют главным образом электроны, занимающие именно внешние или близкие к ним орбитали. [11]
К донорно-акцепторной примыкает координативная дативная связь, при которой один и тот же атом может быть одновременно и донором и акцептором электронов. Атом хлора, в отличие от своего аналога фтора, имеет свободные Sd-орбитали. [12]
 |
Бороводороды ( бораны. [13] |
Четвертой валентностью здесь считается дативная связь ( см. стр. Свою координационную четырех-еалентность бор осуществляет также в трифенилборе ( СвН5) 3В, который способен присоединять один атом натрия. [14]
Разновидностью координативной связи является дативная связь, при которой один и тот же атом может быть и донором и акцептором. В этом отношении представляет интерес механизм образования молекул галогенов, в которых энергия связи должна уменьшаться от фтора к иоду. Из сравнения действительных значений энергий связи ( в кдж / моль) F2 ( - 156 5), С12 ( - 239 3), Вг2 ( - 190 0) и Т2 ( - 148 5) видно, что энергия связи в молекуле фтора меньше, чем в молекуле хлора. [15]
Страницы: 1 2 3 4 5