Дативная связь
Cтраница 3
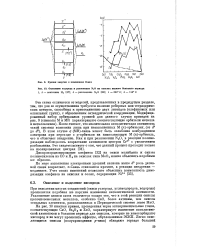 |
Уровни энергии в комплексах Косее.| Окисление водорода и разложение N O на окислах первого большого периода. [31] |
По мере заполнения электронами уровней катиона выше d3 роль дативной связи возрастает. Связь становится прочнее, а реакция внедрения - медленнее. [32]
Наличие л-компонента в связи металл - лиганд ( обычно это дативная связь) препятствует вращению лиганда. Более того: так как дативная и донорно-акцепторная связь взаимно усиливают друг друга, такой поворот снижает и прочность о-компоненты связи металл - лиганд. [33]
Упрочнение связи при комбинации мягких соединений во многих случаях объясняется образованием дативной связи. После образования донорной связи за счет пары электронов основания я-электроны кислоты-акцептора заселяют незаполненные орбитали основания-донора. [34]
Чатта [65, 68] в координационную химию было введено представление о так называемой дативной связи, обусловленной переходом электронной пары центрального иона на d - или и-орбиту лиганда. Второе и третье обстоятельства ясно продемонстрировали, что, несмотря на огромную ценность обобщения И. И. Черняева, не всегда можно пренебрегать другими видами взаимного влияния составных частей комплексной частицы. Уклонение от закономерностей, установленных для диаквоионов, было обнаружено лишь для соединений, кислотные свойства которых обусловлены диссоциацией лигаидов типа RH, связанных с платиной посредством азота. [35]
Координированные бром - или хлор-атомы способны к образованию такой тс-связи ( дативной связи), а молекулы амина к этому не способны. Если принять, что транс-влияние связано с образованием - связей, то уменьшение числа лигандов, способных к образованию - связей, должно повышать транс-активность остальных координированных лигандов. [36]
Полагают, что в этом ряду усиливается тенденция лигандов к образованию дативной связи. [37]
 |
Схема перекрывания орбиталей платины и этилена при образовании t - комплекса типа соли Цейзе. [38] |
Итак, для образования этой дополнительной ( с точки зрения металла) дативной связи л-типа требуются электроны на d - орбиталях металла. Вот почему именно элементы концов больших периодов ( Ni, Pd, Pt, Си, Ag, Аи) с заполненными или почти заполненными d - уровнями способны образовать олефиновые л-комплексы. [39]
В соответствии с трактовкой Е. М. Шусторовича, в комплексах первой группы преобладающей должна быть дативная связь с М на и-орбиту NO. Эффективность такой связи увеличивается с уменьшением угла. [40]
 |
Изменение каталитической активности окислов металлов 4-го периода по выходу продукта в реакции гидролиза синильной кислоты. [41] |
При каталитической гидратации и гидрохлорировании ацетилена в присутствии окислов и солей щелочноземельных металлов дативная связь катиона с молекулой С2Н2 образоваться не может из-за отсутствия наружных заполненных d - орбит. Действительно, ряд уменьшения активностей окислов, фосфатов и других веществ в реакциях ацетилена: Mg2 Са2 Sr2 Ва2 совпадает с рядом уменьшения отношения е / r катиона. [42]
С этой точки зрения координация лиганда, который обладает большей тенденцией к образованию дативной связи, должна уменьшать трансактивность первоначальных лигандов. [43]
Первый фактор они оценивают окислительно-восстановительными потенциалами лигандов и центрального атома, а величину дативной связи определяют сравнением констант устойчивости комплексов, образованных центральным атомом в окисленном и восстановленном состояниях. На основе этих предположений и допущений была выведена формула, которая позволяет вычислить коэффициент трансвлияния. [44]
Координационные поверхностные соединения образуются как за счет донорно-акцепторных, так и за счет дативных связей катализатор - МОС. Моделью последнего типа комплексов могут служить полихелаты, например полимерный трцс - ( дибензоилметацато) лаптан, в котором атомы лантана являются формально ненасыщенными ( имеют вакантные АО) и образуют координационные связи с атомами кислорода соседних лигандов, сравнительно легко разрываемые термически, фотохимически или механохимически. [45]
Страницы: 1 2 3 4 5