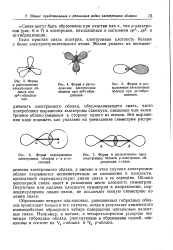
Неполярная связь
Cтраница 1
Неполярная связь - это ковалентная связь между атомами с одинаковой электроотрицательностью ( ЭО); при образовании неполярной связи область перекрывания электронных облаков находится на одинаковом расстоянии от ядер обоих атомов. [1]
Неполярная связь см. Связь ковалептная Неравенство Клаузиуса 311 ел. [2]
Неполярная связь образуется между атомами одного и того же элемента. Связь между атомами разных элементов всегда в известной мере полярна. Это обусловливается различием электроотрицатель-ностей атомов и их размерами. По Полннгу, с увеличением разности электроотрицательностей атомов элементов растет степень ионностн связи. В оксидах щелочных металлов, например, степень ионности велика, а в С12О7 - незначительна, связь ( С1 - О) близка к неполярной. В образующихся полярных молекулах центры тяжести положительных и отрицательных зарядов не совпадают. Так, в молекулах галогеноводородов ( Н - Г) общая электронная пара смещена в сторону более электроотрицательных атомов галогенов ( Г), что приводит к появлению у них эффективного отрицательного заряда ( Н б - Г 6), в Н 0 2 - С1 - 0 - в единицах заряда электрона. Следовательно, молекулы галогеноводородов и им подобные структуры являются диполями; они полярны, состоят из двух равных по величине и противоположных по знаку зарядов ( 6 и - б), находящихся на расстоянии / - длины диполя. [3]
Неполярная связь типична для молекул, состоящих из атомов одного и того же элемента или элементов, очень близких между собой по химическим свойствам. В этом случае электронная пара ( связующий электронный дублет) в равной степени обслуживает остовы обоих атомов, образующих молекулу данного вещества. [4]
Облако неполярной связи имеет в указанном месте плоскость симметрии. Отсутствие или наличие плоскости симметрии в направлении, перпендикулярном линии связи, не исключает осевую симметрию по линии связи. [6]
 |
Схематическое изображение различных по полярности молекул ( ионные молекулы - крайне редкое состояние. [7] |
Для неполярных связей Z0, и дипольный момент также равен нулю. [8]
Облако неполярной связи имеет в указанном месте плоскость симметрии. Отсутствие или наличие плоскости симметрии в направлении, перпендикулярном линии связи, не исключает осевую симметрию по линии связи. [9]
Различают полярную и неполярную связь между атомами в молекулах. [10]
По малополярным и неполярным связям распад на ионы, как правило, не происходит. [11]
 |
Схема перехода полярной структуры в ионную. [12] |
По малополярным и неполярным связям распад на ионы, как правило, не происходит. [13]
С - неполярная связь и В - промежуточное состояние, которое, вероятно, предшествует диссоциации молекулы Js на коны и на свободные атомы. Кроме того, согласно Льюису, два связывающих электрона в форме С в зависимости от обстоятельств могут больше приближаться то к одному, то к другому атому, создавая частичную полярность молекулы, что в конечном итоге тоже может привести к ионизации молекулы. Однако не следует считать, что все молекулы одновременно находятся в одном состоянии; напротив, некоторые молекулы высокополярны, некоторые почти не-полярны, а другие представляют все переходы между этими двумя типами [ 24, стр. Однако если молекулы построены несимметрично, как, например, BrJ, то распределение электронов в молекулах вещества будет таким, что в массе будут преобладать молекулы со сдвигом электронов к какому-либо одному атому, например в молекуле BrJ - к атому брома. [14]
Слабая и относительно неполярная связь Hg - С [106] может легко расщепляться гомолитически. Как и следовало ожидать, для ртутьорганических соединений известны разнообразные свободно-радикальные реакции, большая часть которых представляет собой бимолекулярное замещение у атома ртути. [15]
Страницы: 1 2 3 4