Неполярная связь
Cтраница 4
При изучении химической связи формируются понятия о ковалентной полярной и неполярной связи, о а - и я-связях, о ионной связи и поведении ионов в растворах, а также о металлической связи и строении молекул органических веществ. Особое внимание уделяется при этом единой электронной природе любой химической связи, образованной частичным перекрыванием электронных облаков. Именно поэтому изучение начинается с рассмотрения ковалентной неполярной связи, затем полярной и ионной - как крайнего случая полярной связи. Опорным при изучении полярной связи является понятие об электроотрицательности элементов, которое дает ключ к пониманию причин смещения электронных пар. [46]
 |
Схема опыта Холла. [47] |
При перекрывании внешних орбиталей в отличие от образования валентной неполярной связи не наблюдается направленного взаимодействия между атомами, а электроны мигрируют от одного атома к другому, осуществляя металлическую связь. [48]
Вероятно, однако, что удовлетворительные результаты определения энергии неполярной связи ( как в § 12.6 для определения Д) можно аолучить и при соответствующем использовании данных для соединений, содержащих наименьшее возможное число атомов. Это мы вынуждены делать обычно, и поэтому мы будем поступать так же в случае соединений углерода. [49]
 |
Схемы полярной и неполярной связи. [50] |
Несколько грубо можно так пояснить постепенный переход от полярной к неполярной связи. В типичном полярном соединении валентные электроны остаются связанными со своими ионами; в переходных типах они вследствие взаимной поляризации все больше и больше перетягиваются от аниона к катиону, а в типичном неполярном соединении они в одинаковой степени принадлежат обоим ионам, вращаясь одновременно вокруг обоих ядер и осуществляя этим химическую связь. [51]
Кривые; электрического потенциала для случая: о-ассоциации ионон и б-образования неполярной связи. [52]
Однако факт отсутствия растворимости не может еще служить доказательством наличия у соединения неполярной связи. Так, энергия связи, например, у окислов настолько больше энергии связи щелочных галогенидов, что диэлектрическая постоянная воды уже недостаточна для отрыва ионов от кристалла. [53]
Изложенные данные интересны тем, что они показывают возможность гетеролитического расщепления даже совершенно неполярной связи при ее - взаимодействии с достаточно сильным основанием. [54]
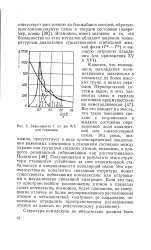 |
Зависимость / от sin 9Д деленной доли ковалент-для германия ной или гомеополярной. [55] |
Получающаяся в результате этого структура становится устойчивее за счет относительной стабильности и направленности неполярной связи. [56]
В органических соединениях преобладает другой вид связи, получивший наименование ковалентнои, гомеополярнои или неполярной связи. Возникновение этой связи характеризуется тем, что образование устойчивой электронной конфигурации у взаимодействующих атомов достигается вхождением равного числа ( одного или нескольких) электронов каждого из реагирующих атомов в электронную оболочку другого без ухода из электронной оболочки своего атома. Образуются одна или несколько электронных пар ( дублетов), причем в состав каждой из них входит по одному электрону от каждого атома. Тем самым дублет, входя одновременно в электронные системы обоих атомов, становится общим для них. Электронные системы обоих атомов переплетаются между собой, и атомы находятся друг к другу ближе, чем в случае ионной связи. [57]
В органических соединениях преобладает другой вид связи, получивший наименование ковалентной, гомеополярной или неполярной связи. Возникновение этой связи характеризуется тем, что образование устойчивой электронной конфигурации у взаимодействующих атомов достигается вхождением равного числа ( одного или нескольких) электронов каждого из реагирующих атомов в электронную оболочку другого без ухода из электронной оболочки своего атома. Образуются одна или несколько электронных пар ( дублетов), причем в состав каждой из них входит по одному электрону от каждого атома. Тем самым дублет, входя одновременно в электронные системы обоих атомов, становится общим для них. Электронные системы обоих атомов переплетаются между собой, и атомы находятся друг к другу ближе, чем в случае ионной связи. [58]
Страницы: 1 2 3 4