Неполярная связь
Cтраница 2
Слабая и относительно неполярная связь Hg-С [106] может легко расщепляться гомолитически. Как и следовало ожидать, для ртутьорганических соединений известны разнообразные свободно-радикальные реакции, большая часть которых представляет собой бимолекулярное замещение у атома ртути. [16]
 |
Зависимость степени ионности связи q / e от разности электроотрицательноетей элементов АЭО, атомы которых образуют данную связь. [17] |
Электронная пара неполярной связи в равной степени принадлежит связываемым атомам. [18]
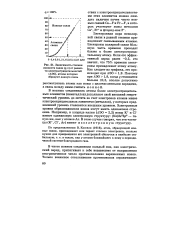 |
Зависимость степени ионности связи ( q / e от разности электроотрицательностей ( ДЭО, атомы которых образуют данную связь. [19] |
Электронная пара неполярной связи в равной степени принадлежит связываемым атомам. Электроны полярной связи большую часть времени проводят ближе к более электроотрицательному атому. Если его эффективный заряд равен - 0 5, это значит, что 75 % времени электроны принадлежат этому атому. Поэтому при АЭО 1 9, когда q становится больше 0 5, вполне допустимо рассматривать атомы как ионы с целочисленными зарядами, а связь между ними считать ионной. [20]
 |
Зависимость степени ион-ности связи ( q / e от разности элек-троотрицательностей элементов ( Ах, атомы которых образуют данную связь. [21] |
Электронная пара неполярной связи в равной степени принадлежит связываемым атомам. Электроны полярной связи большую часть времени проводят ближе к более электроотрицательному атому. Если его эффективный заряд равен-0 5, это значит, что 75 % времени электроны принадлежат этому атому. Поэтому при Ах 1 9, когда q становится больше 0 5, вполне допустимо рассматривать атомы как ионы с целочисленными зарядами, а связь между ними считать ионной. [22]
В случае неполярной связи общие пары электронов в равной мере принадлежат обоим соединяющимся атомам и находятся на равных расстояниях от ядер двух атомов. [23]
Молекулы с неполярными связями являются неполярными молекулами. [24]
 |
Кристаллическая решетка алмаза. [25] |
Они связаны прочными ковалент-ными неполярными связями. [26]
 |
Зависимость Х0бм органических катионов на ионы водорода на сульфокатио-ните КУ-1 т степени заполнения адсорбционной емкости ( М органическими ионами. [27] |
В этом случае замена соседних неполярных связей С-ОН или SiOH на полярные С-О К и SiCr К ослабляет способность водорода соседних гидроксильных групп к диссоциации. [28]
Такой метод неприменим к неполярным связям, а также в тех случаях, когда растворитель преимущественно ассоциируется с другой частью молекулы, вследствие чего ожидаемый сдвиг исследуемой полосы не наблюдается. Однако, несмотря на эти ограничения, метод смещения частот под влиянием растворителей имеет большие возможности для идентификации групповых частот и установления структуры. [29]
У четырехвалентных элементов при неполярных связях обнаруживается опять равномерное распределение всех валентных электронов. Связи располагаются в этом случае в направлении от центра правильного тетраэдра к его вершинам. [30]
Страницы: 1 2 3 4