Соседняя связь
Cтраница 2
Энергии связей более чувствительны к влиянию соседних связей молекулы, чем остальные физические свойства, поэтому отклонения от правила аддитивности здесь более резко выражены. У трех изомерных пентанов теплоты сгорания и образования отличаются друг от друга на несколько килокало. [16]
Энергии связей более чувствительны к влиянию соседних связей молекулы, чем остальные физические свойства, поэтому отклонения от правила аддитивности здесь более резко выражены. [17]
Индуктивный эффект передается не только на соседнюю связь, но может, постепенно ослабевая, распространяться вдоль цепи на несколько ее звеньев. [18]
Вследствие малости расстояния между указанными двумя соседними связями выходящие по ним электронные пучки будут отталкиваться друг от друга и давать на экране вместо накладывающихся одно на другое круглых пятен ( как в случае близко сидящих молекул простых газов) два раздельных пятна в форме фасольных долек, обращенных плоскими участками внутрь. Вращение этих пятен вокруг оси симметрии фигуры может давать изображение молекулы в виде светлого кружка с темным центром. [19]
В рассмотренных примерах при изменении взаимных расположений соседних связей общая конформация макромоле-кулярного клубка остается статистической и изменения ее температурного коэффициента носят линейный характер. Однако при повышении температуры появляется возможность возникновения определенной упорядоченности в расположении транс - и гош-конфор. [20]
В наибольшей мере этот эффект проявляется на соседней связи, но может также сказываться и на удаленных связях. В рассматриваемом примере поляризация связи С-С вызывает также незначительную поляризацию трех связей С - Н в метильной группе. Часто очень трудно разделить эти два эффекта, но во многих случаях это было сделано; при этом, как правило, исходили из того факта, что эффект поля зависит от геометрии молекулы, а индуктивный эффект зависит только от природы связей. Например, в показанных ниже изомерах 1 и 2 [32] индуктивные эффекты атомов хлора, влияющие на положение электронов в группе СООН ( а следовательно; и на кислотность, см. гл. [21]
Очевидно, что при наличии всего двух соседних связей свободного вращения не может быть; оно возникает, если есть не менее трех последовательных связей. [22]
Образовавшиеся дефицитные положения ( дырки) занимают электроны соседних связей, и таким образом осуществляется перенос электронов. [23]
Простейшим случаем химической связи, изолированной от влияний соседних связей, является двухатомная молекула, на примере которой удобно рассмотреть причины, вызывающие появление электрического дипольного момента. [24]
Карбоксильная группа хотя и увеличивает кислотность атома Н соседней связи С - Н, но не имеет практического значения. Дело в том, что при взаимодействии с основанием в первую очередь отщепляется атом водорода карбоксильной группы. Образующийся карбоксилатный анион уже не оказывает активирующего действия на связи С - Н, поскольку для него характерен не - / -, а / - эффект и, кроме того, он не способен к сопряжению со свободной электронной парой, которая могла бы появиться на соседнем атоме углерода при отщеплении протона. [25]
Любой электрический заряд на атоме индуцирует диполь на соседних связях. Этот эффект, известный под названием индукционного эффекта, может распространяться вдоль насыщенной цепи, но быстро тормозится и становится незначительным с увеличением длины цепи. [26]
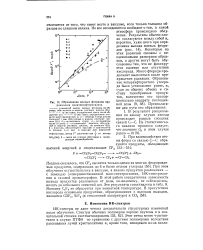 |
Образование ионных фторидов при. [27] |
В результате расщепления по закону случая иногда происходит разрыв соседних связей С-С. [28]
Поскольку на незаполненную связь легко переходят валентные электроны с соседних связей, чему способствует тепловое движение в кристалле, место, где отсутствует валентный электрон, хаотически перемещается по решетке. [29]
В наборе III локализованные валентные МО частично орто-гонализованы с соседними связями, как для набора I, но 2s - AO, использованные при построении гибридов, ортогонализованы к ls - АО того же центра. Ортогонализация обусловливает наличие узлов на валентных МО в области ядер. [30]
Страницы: 1 2 3 4