Простая углерод-углеродная связь
Cтраница 1
Простая углерод-углеродная связь способна вращаться вокруг своей оси, поэтому происходит постоянное изменение ( конформация) формы молекул. [1]
Простая углерод-углеродная связь способна вращаться вокруг своей оси, поэтому происходит постоянное изменение ( конформа-ция) формы молекул. Вследствие внутреннего движения в молекулах углеродные цепи могут образовать кольца ( циклы), в результате возникают алициклические соединения или циклоал-каны. [2]
В случае простой углерод-углеродной связи векторы обеих углеродных валентностей лежат на одной прямой и поэтому обе системы углеродных атомов могут свободно вращаться вокруг этой прямой. Конечно обе углеродные системы определенным образом пространственно расположены относительно друг друга. Направляющее влияние оказывают другие связанные с углеродными атомами группы, которые и обусловливают стабильное состояние всей системы. [3]
В случае простой углерод-углеродной связи векторы обеих углеродных валентностей лежат на одной прямой п поэтому обе системы углеродных атомов могут свободно вращаться вокруг этой прямой. Конечно обе углеродные системы определенным образом пространственно расположены относительно друг друга. Направляющее влияние оказывают другие связанные с углеродными атомами группы, которые и обусловливают стабильное состояние всей системы. [4]
 |
Образование трех гибридных зр2 - орбиталей. [5] |
Энергия разрыва простой углерод-углеродной связи составляет примерно 352 кДж / моль, а для двойной ОС связи она равна 587 кДж / моль. Электроны, участвующие в тг-связывании, слабее удерживаются ядрами углерода, поэтому поляризуемость этой связи гораздо выше, чем ст-связи. [6]
Энергия разрыва простой углерод-углеродной связи составляет примерно 352 кДж / моль, а для двойной С С-связи она равна 587 кДж / моль. Прочность п-связи составляет 587 - 352235 кДж / моль, что значительно меньше, чем освязи ( ср. Электроны, участвующие в я-связывании, слабее удерживаются ядрами углерода, поэтому поляризуемость этой связи гораздо выше, чем о-связи. [7]
 |
Различные способы изображения трехмерного расположения связей вокруг атома углерода в алканах. [8] |
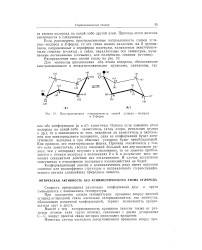
Одним из свойств простой углерод-углеродной связи является возможность относительно свободного вращения вокруг этой связи. Нетрудно представить себе, что, например, верхняя левая метильная группа в молекуле пропана, схематически изображенной на рис. 24.4, вращается относительно остальной структуры. Движения такого типа осуществляются в алканах при комнатной температуре с очень большой скоростью. В результате алканы с длинными цепочками постоянно совершают внутренние движения, приводящие к изменению их формы; нечто подобное происходит с металлической цепочкой при встряхивании. [9]
Можно исключить свободное вращение вокруг простой углерод-углеродной связи промежуточного карбониевого иона, если допустить, что сначала присоединение бром-катиона Вг происходит сразу к обоим углеродным атомам двойной связи. Последующая атака бром-анионом должна, следовательно, происходить с противоположной стороны двойной связи. [10]
Это приводит к значению энергии простой углерод-углеродной связи в углеводородах, равному 83 ккал. С другой стороны, разница в длинах углерод-водородной связи в метане и других углеводородах объясняется различием прочности указанных связей. При таком расчете величину энергии углерод-углеродной связи принимают близкой к найденной для алмаза ( 85 ккал) вследствие близости между длинами этих связей в углеводородах и расстоянием между атомами углерода в алмазе. [11]
Это приводит к значению энергии простой углерод-углеродной связи в углеводородах, равному 83 / скал. С другой стороны, разница в длинах углерод-водородной связи в метане и других углеводородах объясняется различием прочности указанных связей. При таком расчете величину энергии углерод-углеродной связи принимают близкой к найденной для алмаза ( 85 ккал) вследствие близости между длинами этих связей в углеводородах и расстоянием между атомами углерода в алмазе. [12]
 |
Пространственная направленность связей углерод - водород. [13] |
При достаточно низких температурах вращение вокруг простой углерод-углеродной связи настолько затормаживается, что молекулы, обладающие различной конформацией, теряют возможность превращаться друг в. [14]
Наибольшая энергия требуется для возбуждения электронов простой углерод-углеродной связи. Соответственно предельные углеводороды поглощают в области ниже 200 нм. Несколько меньшая энергия необходима для возбуждения электронов других простых связей, в которых, кроме углерода, имеются гетероатомы, содержащие неподеленные пары электронов. Но поглощение спиртов и простых эфиров, аминов и их алкиль-ных производных находится еще в области около 200 нм. Молекулы, содержащие атомы галогена, поглощают уже в более длинноволновой области, и сдвиг тем больше, чем в большей степени поляризовано электронное облако галогена. Для бромистых производных оно лежит в области 200 - 230 нм, а иод-замещенные поглощают в области 270 - 350 нм. [15]
Страницы: 1 2 3 4