Взаимодействие - заместитель
Cтраница 4
Представляет интерес сравнение стабильности 1 2 - и 1 3-диак - сиальных изомеров. В 1 2-изомере диэкваториальные заместители относительно близки друг к другу и, если они достаточно велики, вступают в стерическое взаимодействие, выталкивая частично друг друга в аксиальное положение. В случае 1 3-изомеров взаимодействие диэкваториальных заместителей уже невозможно, в то время как аксиальные заместители находятся в таком положении, что очень близко подходят друг к другу. Согласно расчетам Питцера транс - 1 2-диметилциклогексан содержит при комнатной температуре небольшое, но вполне определенное количество диаксиальной формы. [46]
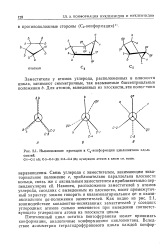 |
Ньюменовские проекции в С3 - конформации циклопентана вдоль. [47] |
Связь углерода с заместителем, занимающим экваториальное положение е, приблизительно параллельна плоскости кольца, связь же с аксиальным заместителем а приблизительно перпендикулярна ей. Наконец, расположение заместителей у атомов углерода, соседних с выведенным из плоскости, носит промежуточный характер: можно говорить о квазиэкваториальном qe - и квазиаксиальном ga - положении заместителей. Как видно из рис. 2.1, взаимодействие ковалентно-несвязанных заместителей у соседних углеродных атомов сильно изменяется при выведении соответствующего углеродного атома из плоскости цикла. [48]
В некоторых случаях понижение АН обусловлено уменьшением водородных связей или дипольного взаимодействия в результате полимеризации. Существенная стабилизация таких мономеров, как акриловая кислота и акриламид, обусловлена сильным межмолекулярным взаимодействием. В полимере оно не играет заметной роли, так как из-за стерических факторов взаимодействие заместителей не может проявиться в достаточной степени. [49]
В молекуле двухиодистого фосфора определены валентные углы и расстояния между атомами фосфора и иода. Изучены ИК - и УФ-спектры двухиодистого фосфора. Расчет потенциальных барьеров внутреннего вращения в тетрагалогендифосфинах - двухиоди-стом и двуххлористом фосфорах - в термах ван-дер-ваальсова взаимодействия заместителей [27], проведенный Боголюбовым, также предсказывает существование этих соединений в растворе при комнатной температуре преимущественно в транс-форме. [50]
Применение модифицированного уравнения Гаммета к соединениям с заместителями в бензольном кольце почти всегда дает положительную величину ря, изменяющуюся от 0 02 до 0 37 в. Активирующее действие электро-ноакцепторных заместителей обусловлено двумя причинами. Вторая причина состоит во взаимодействии заместителя с реакционным центром в самом реагенте. Полярографически восстанавливаемые группы ( карбонильная, нитро -, галогены, азо -) сами являются электроноакцепторными, поэтому при их взаимодействии с электроноакцепторными заместителями происходит дестабилизация реагента. С другой стороны, при взаимодействии электронодонор-ных заместителей с восстанавливающейся группой реагент стабилизируется и становится менее реакционноспособным. [51]
Все это позволяет заключить, что именно заместитель R, а не атом железа сопряжен с я-системой циклопентадиеново-го фрагмента; влияние на атом железа передается по чисто индукционному механизму. Добавочным подтверждением этого вывода служат результаты корреляции влияния замести-телей типа CH2R на равновесие рассматриваемой реакции. Случай аналогичен рассмотренной Экснером реакционной серии ионизации а-замещенных толуиловых кислот. Отключение заместителя R от циклопентадиенильной я-системы устраняет М - составляющую и оставляет лишь индукционные члены взаимодействия заместителя с реакционным центром. [52]
Однако к уравнению такого же типа можно прийти иначе, чем это было сделано в § 2 гл. Действительно, если предположить, что при условии постоянства всех остальных структурных факторов влияние изменения любого из их числа описывается однопараметровой линейной зависимостью типа Гаммета - Тафта, то для случая одновременного изменения всех факторов мы получим уравнение, по своей форме тождественное уравнению ( II. Ясно также, что обычный аддитивный подход сводится к пренебрежению всеми перекрестными членами в этом уравнении. В предыдущих параграфах этой главы мы видели, что в некоторых специфических случаях такой аддитивный подход не является оправданным из-за наличия существенного взаимного возмущения между различными типами взаимодействия заместителей с реакционным центром. В принципе, как раз такие возмущения и должны учитываться перекрестными членами. [53]
Влияние полизамещения представляет чрезвычайно большой интерес. Такая же картина наблюдается и в случае многих других заместителей. Данную закономерность трудно интерпретировать с помощью одних только резонансных структур; однако Брэлсфорду с сотрудниками [48] удалось дать изящное и вполне удовлетворительное объяснение в рамках простой теории МО. Введение метильной группы они рассматривают как возмущение молекулярной структуры бензола. Степень взаимодействия заместителя с молекулярной орбитой зависит от значения волновой функции в точке, где происходит замещение. Поэтому электронодонорные заместители будут повышать энергию ( дестабилизировать) орбиты, а электро-ноакцепторные, наоборот, понижать ее ( стабилизировать) пропорционально значению волновой функции в точке, где происходит замещение. [54]
Страницы: 1 2 3 4