Взаимодействие - полимерный радикал
Cтраница 2
Если при взаимодействии простейших радикалов вопрос о механизме реакции обрыва сравнительно просто может быть решен путем химического анализа продуктов реакции, то выяснение механизма взаимодействия полимерных радикалов представляет трудную задачу. [16]
 |
Эффективность инициирования (. ин для некоторых мономеров. [17] |
Зависимость скорости радиационной полимеризации от ] / / означает, что полимерные радикалы равномерно распределены в облучаемом объеме и обрыв реакционных цепей преимущественно происходит при взаимодействии полимерных радикалов, образованных в разных треках. Если бы обрыв цепей происходил при взаимодействии радикалов одного трека, то скорость полимеризации была бы пропорциональна первой степени интенсивности облучения, даже при бимолекулярном обрыве цепей. В этом случае увеличение / означало бы увеличение числа изолированных элементарных объемов, в каждом из которых протекает полимеризация. Все эти соображения справедливы для легких частиц, они могут быть не верны для механизма действия тяжелых частиц, например а-частиц. [18]
А и S - концентрации мономера и растворителя; kp, kaa, kar, krr представляют собой соответственно константы скоростей реакций роста цепи, реакции обрыва цепи при взаимодействии полимерных радикалов между собой, полимерного радикала с радикалом, образованным из растворителя, и радикалов, образованных из растворителя, между собой; с - отношение константы скорости реакции, передачи цепи через растворитель к константе скорости реакции радикала растворителя с мономером. [19]
Отклонения от величины 0 5 можно в ряде случаев объяснить инги-бирующим действием растворителя или примесей, содержащихся в полимеризационной среде, так как обрыв цепей происходит частично и за счет взаимодействия полимерного радикала с растворителем и примесями. [20]
Бонсалл, Валентайн, Мелвилль [1050], показали, что отрыв цепей при полимеризации метилметакрилата без ингибитора осуществляется в результате реакции диспропорционирования полимерных радикалов, а в присутствии ингибитора - за счет взаимодействия полимерного радикала с ингибитором. [21]
На основании кинетических измерений Мортон, Кала и Пи-ирма [607] обнаружили, что скорость поперечного сшивания при полимеризации изопрена меньше, чем в случае бутадиена; авторы объясняют этот факт стерическими затруднениями при реакции взаимодействия полимерного радикала с остаточными двойными связями молекулы полиизопрена. [22]
А о и Ам - константы скорости обрыва и передачи цепи через мономер; и - скорость полимеризации; М - концентрация мономера, X - концентрация ингибитора; X - доля реакции диспропорционирования при взаимодействии полимерных радикалов между собой; ( - коэффициент, величина которого определяется механизмом реакции ингибирования. [23]
Значения ц, меньшие химического значения, объяс - няются на основе гипотезы о горячих радикалах ( см. стр. При взаимодействии полимерного радикала с молекулой ингибитора происходит образование горячего радикала, который может или регенерировать реакционную цепь или дезактивироваться. Если считать Хх 1 то i должно равняться удвоенной вероятности дезактивации горячего радикала. В рамках рассматриваемой концепции необходимо различать регенерацию цепи через холодные и горячие радикалы. Первый процесс зависит от концентрации ингибитора и от температуры, тогда как второй процесс не зависит от этих параметров. Авторы цитированных работ приводят различные соображения в пользу выдвинутого ими объяснения малых стехиометрических коэффициентов. [24]
В момент затвердевания каучуковых частиц вязкость их резко возрастает. Согласно существующим представлениям константа скорости взаимодействия полимерных радикалов при этом должна уменьшаться. Каким образом возрастает скорость сшивания каучуковых молекул, остается не ясным. [25]
Холт и Симпсон [ I310I исследовали кинетику полимеризации диал лшювых эфиров следующих дикарбоновых кислот: тере1 фталевой, о-фталевой, изофталевой, дифеновой, 1 8-нафтеновой, угольной, щавелевой, малоновой, пробковой, глутаровой, ади-пиновой, азелаиновой, себациновой, ди-р-металлилфталата и ди-р-металлилкарбоната при 70 - 100 в присутствии перекиси бензола в качестве инициатора. Авторы показали, что при полимеризации диаллилтерефталата, в результате взаимодействия полимерного радикала с двойной связью чужой полимерной молекулы, происходит образование многократных поперечных связей между двумя цепями. Во всех остальных случаях преобладает реакция циклизации: взаимодействие полимерного радикала с двойной связью своей молекулы. [26]
При облучении стирола, метилметакрилата и винилацетата в массе вплоть до 8 % превращения полимеризация протекает с постоянной скоростью, пропорциональной квадратному корню из интенсивности облучения. Эта зависимость указывает на то, что обрыв реакционных цепей происходит путем взаимодействия полимерных радикалов друг с другом. [27]
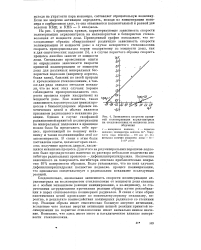 |
Зависимость скорости привитой полимеризации акрил онитрила на стекловолокнах от мощности дозы облучения. [28] |
Следовательно, аномальная зависимость скорости полимеризации акрилонитрила на мелкопористом стекловолокне от мощности дозы связана не с особым механизмом реакции инициирования, а по-видимому, со сте-рическими затруднениями протекания реакции обрыва путем рекомбинации в порах стекловолокна полимерных радикалов. В связи с этим обрыв кинетических цепей происходит по мономолекулярному механизму, вероятно, в результате взаимодействия полимерных радикалов со стенками пор. Реакция обрыва имеет относительно большую энергию активации, вследствие чего полная энергия активации цепной реакции привитой полимеризации на пористом стекловолокне имеет аномально низкое значение. Возможно, что здесь имеет место и каталитическое влияние поверхности стекловолокна. [29]
Средняя длина полимерных цепей, как это следует из ее определения, равна числу заполимеризовавшихся молекул мономера, деленное на число образовавшихся за это время молекул полимера. Если реакция передачи цепи отсутствует, то скорость образования полимерных молекул может быть выражена через скорость взаимодействия полимерных радикалов. Для установления связи между этими величинами необходимо принять во внимание два обстоятельства. [30]
Страницы: 1 2 3 4