Взаимодействие - карбоксильная группа
Cтраница 1
Взаимодействие карбоксильных групп с аминогруппами при отсутствии катализаторов начинается при температурах выше 150 С. Несмотря на высокие температуры, процесс протекает сравнительно медленно ( константы скоростей 1Q - 5 - 10 - 3 моль-л - с 1) и носит равновесный характер. Более реакционноспособные ангидриды кислот могут взаимодействовать с диаминами при невысоких температурах; при этом равновесный характер процесса сохраняется [ 6, с. [1]
Взаимодействие карбоксильной группы и бензольного кольца приводит к перераспределению электронной плотности. Ароматическое кольцо, имеющее электрофильный характер, несколько оттягивает электронное облако от углерода карбонила, чем ослабляется связь между кислородом и водородом гидроксила. Этим и объясняется большая величина констант диссоциации этих кислот. [2]
Взаимодействие карбоксильной группы с диаминами ( такими как этилендиамин, гексаметилендиамин), с полиаминами или их карбонатами, боратами и другими солями [58; 68] протекает с образованием либо ионных ( аммониевых солей), либо неионизированных ( амид-ных) группировок. [3]
При взаимодействии карбоксильных групп эластомера с поли-изоцианатами также возникают амидные поперечные связи. [4]
В результате взаимодействия карбоксильных групп с оксидами металлов образуются почти исключительно внутримолекулярные средние соли, которые в неполярной среде каучука объединяются в микроагрегаты. Образование последних достаточно вероятно, так как реакция имеет гетерогенный характер, обусловленный тем, что оксиды металлов не растворяются в каучуке. Солеобра-зованию предшествует адсорбция карбоксильных групп на поверхности дисперсных частиц оксида. По мере протекания реакции полярность адсорбированных групп возрастает, а их стремление к десорбции уменьшается. Адсорбционные взаимодействия достаточно сильны, чтобы микроагрегаты сохранялись при обычных температурах. Однако при повышении температуры эти взаимодействия ( слабые вулканизационные связи) быстро ослабляются и прочностные свойства вулканизатов резко ухудшаются. [5]
Метод основан на взаимодействии карбоксильных групп по-лигликольтерефталатов со спиртовым раствором гидроксида калия и определении последнего при титровании на спектрофотометре при длине волны 602 нм. [6]
Пептидная связь возникает при взаимодействии карбоксильной группы одной аминокислоты и аминогруппы другой. [7]
Выше было показано, что в результате взаимодействия карбоксильной группы одной молекулы аминокислоты с аминогруппой другой молекулы образуется дипептид. [8]
Таким образом, при последовательном замещении метальных групп атомами хлора сила взаимодействия карбоксильных групп анионов с молекулами воды уменьшается. Следует поэтому ожидать, что ион триметилацетата будет стремиться перейти в разбавленную фазу раствора сильнее, чем более слабое основание - ион метилдихлорацетата, который в свою очередь будет стремиться перейти в разбавленную фазу раствора сильнее, чем еще более слабое основание - ион трихлорацетата. [9]
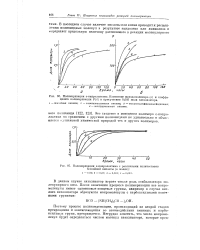 |
Полимеризация е-капролактама. Изменение выхода полимера ( а и коэффициента полимеризации Р ( б в присутствии 0 005 моля катализатора. [10] |
Поэтому процесс поликонденсации, происходящий на второй стадии превращения и заключающийся во взаимодействии аминных и карбоксильных групп, прекращается. [11]
СООН ( СН2) ПСООН, где п достигает такой величины, при которой взаимодействием карбоксильных групп можно пренебречь. [12]
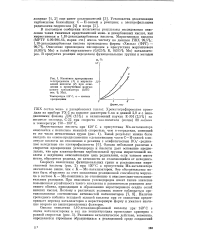 |
Кинетика превращения w - тетрадекана ( 1 и миристи-новой кислоты ( 2 при окислении в присутствии марганцевого катализатора ( 0 035 вес. % Мп. [13] |
Однако небольшое различие в скоростях превращения углеводорода и кислоты дает основание предполагать, что при взаимодействии карбоксильной группы миристиновой кислоты с ведущими окислительную цепь радикалами, если таковое имеет место, образуется радикал, по активности не отличающийся от исходного. [14]
 |
Электронно-микроскопическая структура покрытий ( Х32000, полученных при различных рН. [15] |
Страницы: 1 2 3 4