Дативное взаимодействие
Cтраница 4
СО дополняют конфигурацию атомд металла до строения атома ближайшего благородного газа. Связь СО с металлом в карбонилах очень прочная, так как здесь имеет место донорно-акцепторное и дативное взаимодействие. Связь металл - СО при этом разрывается, но образуется очень прочная кристаллическая решетка металла. [46]
Выше мы подчеркивали, что при образовании тг-комплекса олефина с переходным металлом последний выступает в роли как акцептора, предоставляя вакантные орбитали для л-электронов олефинов ( донорно-акцепторная связь), так и донора, поставляя d - электроны на разрыхляющие орбитали олефина для образования дативной связи. Естественно, что устойчивость тг-комплекса будет тем выше, чем сильнее как донорно-ак-цепторное, так и дативное взаимодействие лиганда с переходным металлом. Если допустить, что до-норные свойства центрального атома металла в меньшей степени сказываются на устойчивости я-комплекса, то можно предположить, что тс-ком-плекс, возникающий в присутствии системы А1 ( шо - С4Н9) 3 TiCl4, более устойчив, а вследствие этого и изомеризационная способность данной системы выше. [47]
Исследованиями установлено, что первым промежуточным соединением является я-комплекс этилен - палладийхлорид. Комплекс образуется за счет донорно-акцепторного взаимодействия, в результате которого атом палладия предоставляет вакантную rf - орбиталь, а пару электронов - соответствующая разрыхляющая молекулярная орбиталь этилена. Дативное взаимодействие также играет существенную роль в процессе образования л-комплекса, так как у центрального атома имеются электроны на я-орбиталях, способные образовывать дативные связи. Этилен при образовании комплекса с палладием ведет себя как донор и акцептор электронов. [48]
Но кроме того, электроны на я ( d) - уровне металла могут быть делокализованы на незанятую дРазР - орбиталь иона CN -, препятствуя накоплению на атоме металла слишком большого отрицательного заряда. Такую связь часто называют дативной связью. Дативное взаимодействие понижает энергию я ( d) - уровня и делает его менее разрыхляющим. [49]
Влияние дативной связи особенно важно при образовании я-комплекса по механизму вытеснения. Взаимодействие не занятых в связях d - электронов центрального атома с разрыхляющими орбиталями ненасыщенного соединения осуществляется на расстояниях, больших, чем те, которые необходимы для осуществления донорно-акцепторной связи. Дативное взаимодействие обеспечивает предварительную ориентацию реагентов и облегчает последующий процесс замещения. [50]
Увеличение кратности связи между комплексообразователем и лигандами за счет образования я-связи повышает устойчивость комплекса, а дативный механизм ее возникновения увеличивает положительный заряд на центральном атоме, что способствует более глубокому проникновению электронных пар лигандов в его оболочку. Это приводит к большему перекрыванию орбиталей комплексообразователя и лигандов, что еще сильнее упрочняет связь и проявляется в ее укорочении. Дативное взаимодействие усиливает ковалентный характер связи, однако ни в коей мере нельзя отождествлять ковалентность связи с ее прочностью, а ионность - со слабостью. Напомним, что прочность связи определяется ее энергией и длиной, но не характером. [51]
Вг, I) практически одинакова, а устойчивость твердых GeF2 повышается с ростом порядкового номера галогена. Стабильность GeF, можно объяснить дативным взаимодействием ( свободные орбиты германия - электронные пары галогена), которое, вероятно, увеличивается от фтора к иоду. [52]
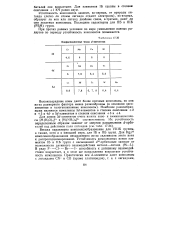 |
Координационные числа ( / - элементов. [53] |
Весьма характерно комплексообразование для VIIIB группы, а также, хотя и в меньшей мере, для 1Б и ПБ групп. Для Hga2 комплексообразование нехарактерно из-за склонности этого иона к диспропорционированию. В ряду F - - СЬ - Вг - - I - способность к дативному взаимодействию возрастает, и в этом же направлении возрастает устойчивость комплексов. [54]
 |
Схема связей этилена с платиной в молекуле соли Цейзе ( а и ртути ( HgSOJ с ацетиленом ( б. [55] |
Роль донорно-акцепторного и дативного взаимодействий в образовании я-комплексов может быть различной в зависимости от природы лигандов и центрального атома. Так, бис-я-циклопентадиенилы вполне устойчивы без дативных связей. В то же время стабильные я-комп-лексы ацетиленов, олефинов и ароматических соединений образуются лишь в тех случаях, когда возможно дативное взаимодействие. [56]
 |
Схема связей этилена с платиной ртути ( HgSO4 с ацетиленом ( б. [57] |
Роль донорно-акцепторного и дативного взаимодействий в образовании я-комплексов может быть различной в зависимости от природы лигандов и центрального атома. Так, б с-я-циклопентадиенилы вполне устойчивы без дативных связей. В то же время стабильные я-комп-лексы ацетиленов, олефинов и ароматических соединений образуются лишь в тех случаях, когда возможно дативное взаимодействие. [58]
Расчеты были выполнены методом CNDO. Сравнение с расчетом для соли Цейзе, выполненным в том же приближении, показывает, что в рассмотренном переходном состоянии электроны переходят к лиганду от атома Pt. Таким образом, совокупность данных, а также прямые оценки заселенности я - МО этилена указывают, что основную роль в стабилизации переходной структуры играет дативное взаимодействие. [59]
Страницы: 1 2 3 4