Зр-орбиталь
Cтраница 1
Зр-орбиталь имеет один узел. [1]
 |
Избежание пересечения типа В. Copyright 1975 by American Chemical Society. [2] |
Зр-орбиталь хлора, направленная к атому натрия. [3]
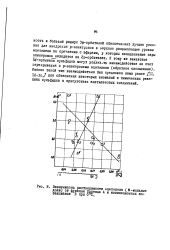 |
Зависимость растворимости ацетилена ( N-мольные доли от функции Лоренца А и ионизационных потенциалов Б при 0 С. [4] |
Зр-орбиталей обеспечивает лучшие условия для внедрения р-электронов в верхние разрыхляющие уровни ацетилена по сравнению с эфирами, у которых неподеленные пары электронов находятся на 2р - орбиталях. Именно такой тип взаимодействия был предложен нами ранее / П, 18 36 7 Для объяснения некоторых аномалий в химических реакциях сульфидов в присутствии ацетиленовых соединений. [5]
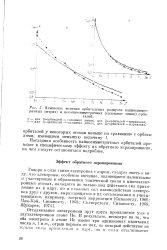 |
Изменение величин орбитальных радиусов кайносиммет-рцчных ( штрих н некайносимметричных ( сплошные линии орбиталей. [6] |
Зр-орбиталей - сплошная линия, для 2р - орбиталей - штриховая. [7]
Зр-орбиталей здесь несколько возрастает. [8]
Зр-орбиталей идентичны соотношениям (3.37) для 2s - и 2р - орбиталей, а также получить аналогичное соотношение для ЗЙ-орбиталей. [9]
Сколько вакантных Зр-орбиталей имеет в стационарном и возбужденном состоянии атом кремния. [10]
На Зр-орбиталях имеется два свободных электрона. Так как в энергетическом отношении 3s и Зр-уровни близки, возможно возбужденное состояние, описываемое формулой Is22s22pe3s1, Зр хЗр уЗр1 с четырьмя валентными электронами. За счет 5р3 - гибридизации они могут образовать четыре связи. Электронная конфигурация атома кислорода s22s22p2x2ply2plz допускает образование о-связей между атомом кислорода и кремния. Поэтому атом Si посредством гибридизации образует с электронами 2р - орбиталей атома кислорода четыре связи. Они направлены к вершинам тетраэдра. В свою очередь атом кислорода, который имеет два свободных электрона ( р-орбйталей), связывается с двумя атомами кремния. Последнее обусловливает возможность образования правильных непрерывных сеток из тетраэдров SiO4 / 2, связанных друг с другом через общие атомы кислорода. Это вызвано существенной вариабильностью характера гибридизации и способа использования свободных орбиталей при образовании связи. Кроме о-связей кислород может образовывать я-связи при наличии гибридизации типов sp2 и sp за счет использования незаполненных орбиталей соседних атомов. У атома кислорода остаются вакантными неподеленные пары 2р и 2s - электронов. [11]
После заполнения всех Зр-орбиталей порядок заполнения следующих орбиталей усложняется. [12]
После заполнения всех Зр-орбиталей порядок заполнения следующих орбиталей усложняется. [13]
Каждая орбиталь перекрывается с од-нократно заполненной атомной Зр-орбиталью хлора. [15]
Страницы: 1 2 3 4 5
