Зр-орбиталь
Cтраница 2
В атоме кремния на Зр-орбиталях имеется только два свободных электрона. [16]
Радиусы некайносимметричных 3s - и Зр-орбиталей, вытесненных псевдо-потенциалом из более глубоких положений, превышают радиусы Зе ( - орбита-лей, начиная с ванадия. Кайносимметрия Зс ( - атомов выражается и в пониженных ( по сравнению с 4d и 5d) энергиях сублимации металлов и в меньшей прочности образуемых ими комплексных соединений. [17]
Фосфор имеет пять электронов на 3s - и Зр-орбиталях, а сера - шесть. Почему же элементы третьего периода могут иметь столько неспаренных электронов, а элементы второго периода нет. Дело заключается в том, что элементы третьего периода имеют сравнительно глубоко лежащие вакантные орбитали такого же размера, как 3s - и Зр-орби-тали, которые также необходимо учитывать: это Зй-орби-тали. Следует подчеркнуть, что не сравнительно низкая энергия этих Зй-орбиталей ( на самом деле, 4s - и 4 / - орбита-ли дают более глубокие уровни энергии, чем Зй-орбитали) позволяет включать их при описании связи, а именно приблизительно такая же протяженность их, как 3s - и 3 / 7-орбиталей. Это означает, что когда мы строим гибридную орбиталъ с помощью 3s -, Зр - и Sd-орбиталей, то каждая из трех компонент вносит существенный вклад в перекрывание этой гибридной орбитали с орбиталями фтора. Если бы Зй-орбитали были более протяженными, чем 3s - или Зр-орбитали, то на расстоянии, при котором перекрывание велико для 3 -орбитали, оно было бы мало для 3s - и Зр-орбиталей, и наоборот, когда 3s - и Зр-орбитали имеют большое перекрывание с орбиталями фтора, Зй-орбиталь должна бы дать малое перекрывание. Энергия возбуждения 2р - 3d для кислорода ненамного больше, чем энергия возбуждения Зр - 3d для серы, но размеры Зй-орби-тали значительно больше, чем размеры 2s - или 2р - орбита-лей, так что любой Зй-характер в гибридной орбитали, содержащей также 2s - и 2р - функции, незначительно увеличивает ее способность к перекрыванию. [18]
Аг - некайносимметричные элементы с повторной уже симметрией своих Зр-орбиталей, пересекающих своей линией радиусов линию 3s довольно далеко по окончании полного заселения вакансии Зр. Более поверхностное положение линии Зр слегка способствует возбуждению Зр-электронов до Sd-состояния. [19]
 |
Переходы между различными атомными орбиталями. [20] |
Электрон Ss-орбитали может быть легко возбужден, так что перейдет на Зр-орбиталь. Возвращение возбужденного электрона обратно на Зз-орбиталь сопровождается излучением фотона в видимой области спектра. Поэтому при внесении натриевой соли в бесцветное пламя газовой горелки она окрашивается в желтый цвет. Под действием высокой температуры пламени наступает термическая диссоциация соли, возбуждение Ss-электрона и эмиссия желтого света ( Я 589 нм) при его возвращении на исходную Ss-орбиталь. [21]
 |
Возникновение энергетических зон кристалла из энергетических уровней атомов по мере их сближения. а - натрий. б - алмаз. [22] |
В кристаллическом натрии происходит перекрывание зон, образованных 3s - и Зр-орбиталями. Для металлов первой группы это перекрывание не играет существенной роли, так как число свободных орбиталей в s - зоне у них велико. Однако такое перекрывание s - и р-зон, наблюдаемое и для металлов второй группы периодической системы элементов, играет важную роль. Атомы этих элементов имеют по два валентных s - электрона, следовательно, все орбитали в s - зоне их кристаллов будут полностью заполнены. Лишь глубокое перекрывание зон, образованных s - и р-орбиталями их атомов, сообщает металлические свойства кристаллам этих элементов. Образование зон проводимости в кристаллах d - элементов обычно сопровождается значительным перекрыванием ns - и ( - 1) а. Это значит, что перекрывание d - орбиталей в таких кристаллах невелико. [23]
 |
Схема, определяющая последовательность заполнения электронами энергетических подуровней атомов. [24] |
Выясним теперь, как располагаются три последние электрона фосфора на его Зр-орбиталях. Заполняют ли они каждую из этих трех орбита-лей поодиночке, или же на одной из них находится пара электронов 1 Принцип максимальной мулъ-типлетности утверждает, что электроны заполняют имеющиеся орбитали очередного подуровня так, чтобы по возможности располагаться на них поодиночке. Дело в том, что, если два электрона находятся на различных орбиталях с неодинаковой пространственной ориентацией, энергия атома оказывается меньшей, чем если бы та же пара электронов оказалась локализованной на общей орбитали, так как в последнем случае возрастает энергия кулоновского отталкивания электронов друг от друга. [25]
 |
Структура молекулы метана. [26] |
Опыт показывает, что в образовании химической связи принимает участие не чистая Зр-орбиталь атома С1, а его гибридная ( 3s Зр) - орбиталь. [27]
В случае образования а-связи у серы за счет перекрывания 3s - или Зр-орбиталей ( без участия Зс - орбиталей) форма гибридных орбиталей остается без изменения. При участии d - орбиталей гибридная орбиталь слегка деформируется. [28]
Для серы, как и для фосфора, характерна слабо выраженная способность Зр-орбиталей образовывать я-связи. [29]
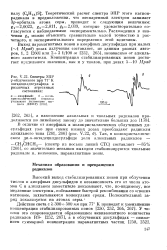 |
Спектры ЭПР у-облученного при 77 К октадецнлдисульфида в различных агрегатных состояниях. [30] |
Страницы: 1 2 3 4 5