Поверхностный избыток
Cтраница 2
Уравнение Гиббса позволяет определить величину поверхностного избытка по уменьшению величины о, вызванному изменением концентрации раствора. Согласно выводу уравнения, Г представляет собой разность между концентрациями адсорбтива в поверхностном слое и в объеме раствора. [16]
Понижение межфазного натяжения является функцией поверхностного избытка адсорбированного вещества и приложенной разности потенциалов. [17]
После того как мы ввели понятие поверхностного избытка, можно приступить к выводу третьего основного уравнения физической химии поверхностей [ первыми двумя являются уравнения Лапласа ( 1 - 7) и Кельвина ( П-20) ], известного как уравнение Гиббса. [18]
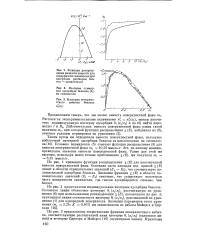
На рис. 3 представлены теоретические функции поверхностного избытка, соответствующие рассчитанной нами изотерме 0 ( ( хг. [20]
Удельная адсорбция, так же как и поверхностный избыток, зависит от положения разделяющей поверхности. [21]
Следует также отметить, что в вычислениях поверхностного избытка нейтральных веществ диффузный слой не фигурирует. [22]
Здесь N - мольная доля; Г - поверхностный избыток; - у - поверхностное натяжение раствора. Индексы 1, 2 и 3 относятся соответственно к воде, октиловому спирту и додецилсульфату натрия; Г2 и Г3 могут быть рассчитаны, так как наклон кривых у - N может быть определен экспериментально. [23]
В поверхностном слое положительным будет избыток ПАВ, тогда как поверхностный избыток воды отрицателен. [24]
Это обычно применяемое приближенное адсорбционное уравнение Гиббса показывает, что поверхностный избыток растворенного вещества пропорционален произведению концентрации на скорость изменения поверхностного натяжения с концентрацией. [25]
Итак, еще раз подчеркнем, что только при локализации поверхностного избытка в пределах адсорбционного монослоя сочетание уравнений (2.15) и (2.19) позволяет рассчитать поверхностную концентрацию органического вещества. [26]
Делахей и Сенда [13] считают ошибочным предположение о том, что поверхностный избыток реагента при наличии специфической адсорбции в области малых заполнений линейно связан с концентрацией в объеме раствора. Если этот вывод справедлив, то должны быть неправильны многие коэффициенты адсорбции металлических ионов, полученные ранее Па. Однако аргументация этих авторов явно ошибочна, когда она применяется к адсорбции компонента, присутствующего в незначительной концентрации в растворе, содержащем большое и постоянное количество индифферентного электролита. [27]
Балашова и сотрудники [ 262 - 267а ] непосредственно измерили) бщий поверхностный избыток катионов и анионов на поляризо-занных платиновых электродах, используя меченые атомы. [28]
Применяя теорему Эйлера об однородных ф-циях, можно получить выражение для поверхностного избытка большого термодинамич. [29]
Разделяющую поверхность можно было бы расположить в фазе раствора таким образом, чтобы поверхностный избыток компонента 1 был равен нулю. При таком расположении разделяющей поверхности поверхностный избыток компонента 2 определяется как Т и его можно найти с помощью методики, изложенной в разд. [30]
Страницы: 1 2 3 4