Алюмосиликагель
Cтраница 2
В противоположность этому, алюмосиликагели, полученные в работе i [68] на основе высокодисперсного силикагеля, не показали ни максимума величины поверхности, ни минимума среднего размера частиц. [16]
В исследованной области спектра алюмосиликагель, силикагель и микропористое стекло имеют одну интенсивную полосу поглощения, принадлежащую первому обертону колебания О - Н гидро-ксилов поверхности адсорбентов. [17]
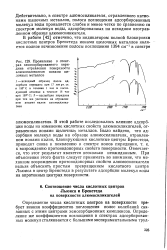 |
Проявление в спектрах хемосорбированного пиридина отравления поверхности алюмосиликагеля ионами щелочных металлов. [18] |
Действительно, в спектре алюмосиликагеля, отравленного катионами щелочных металлов, полоса поглощения адсорбированных молекул воды проявляется слабее и менее четко по сравнению со спектром молекул воды, адсорбированных на исходном неотравленном образце алюмосиликагеля. [19]
Считается, что образцы алюмосиликагелей с высоким содержанием окиси алюминия ( более 80 %) содержат алюминий преимущественно в октаэдриче-ской координации. При дегидратации часть этих комплексов превращается в комплексы, в которых алюминий находится в тет-раэдрической координации. Образцы алюмосиликагеля, содержащие меньше 30 % А12О3, в основном содержат алюминий в тетраэдрической координации. [20]
По мере заполнения поверхности алюмосиликагелей хемосорбирующимся пиридином или хинальдином времена удерживания адсорбатов падают, а пики становятся уже и симметричнее. После модифицирования резко падает специфичность поверхности алюмосиликагелей, меняется порядок выхода адсорбатов из колонки, становится возможным разделение молекул В и D. Ацетон, по-видимому, претерпевает химическое превращение, продукты которого дают хроматограмму с несколькими перекрывающимися пиками. После же модифицирования поверхности этого алюмосиликагеля хинальдином для эфира и даже для этанола при более низкой температуре ( 150) хроматограммы имеют достаточно симметричные пики, а пик ацетона имеет лишь небольшой хвост. На макропористом алюмосиликагеле, модифицированном винилпиридином, хорошо разделилась при 175 смесь пиридина и а -, 3 -, у-пиколинов; на чистой же поверхности алюмосиликагеля все эти вещества хемосорбируются и не выходят из колонки. Необходимо отметить высокую термостабильность хемосорби-рованного покрытия. [21]
В качестве новой характеристики смешанных алюмосиликагелей предлагается термическая устойчивость протонной кислотности ST. ST является функцией концентрации и природы кислотных центров катализаторов. Для реакции разложения муравьиной кислоты, по-видимому, имеется почти линейное соотношение между ST и активностью смешанных гелей. [22]
Адсорбция многих молекул на поверхности алюмосиликагеля приводит к их разложению и образованию новых поверхностных соединений. Алюмосиликагель, подобно окиси алюминия ( см. главу VIII), реагирует со спиртами, альдегидами и кислотами, образуя на поверхности соединения, спектры которых аналогичны спектрам ионов соответствующих кислот. [23]
Разработана методика формирования пористой структуры алюмосиликагеля с целью использования последнего в качестве носителя никелевого катализатора гидрирования гомологов метана. Изменение пористой структуры носителя осуществляется путем пропитки алюмосиликагеля водными растворами HF, NH4F и ( NH4) s Mo7024 - 4H2O с последующим прокаливанием. [24]
С целью исследования структуры каркаса аморфных алюмосиликагелей проведено сравнительное исследование спектров механической смеси окислов SiC2 и А12О3 и синтетического алюмо-шшкагеля, полученного совместным осаждением [12, 13], Было установлено различие в спектрах этих образцов и сделан вывод о том, что алюмосиликатный катализатор не представляет собой механическую смесь окислов, а образует структуру, в которой часть ионов Si4 замещена на А13 в октаэдрической координации. В отличие от этого в работе [14] сделан вывод о существовании алюминия в алюмосиликагеле в тетраэдрической конфигурации. [25]
В случае адсорбции молекул пиридина алюмосиликагелем то -; го же состава установлено [38], что в виде протонированной формы хемосорбируется одна из семи адсорбированных молекул. Это находится в соответствии с различием в основности, молекул аммиака и пиридина. [26]
С увеличением содержания А1203 в алюмосиликагелях, получаемых методом соосаждения, резко ухудшаются показатели структуры пор. Следовательно, задача заключается в разработке способов введения желаемых количеств А1203, позволяющих повысить активность без существенного ухудшения геометрической структуры. [27]
Основная задача в исследовании свойств поверхности алюмосиликагелей как катализаторов реакции крекинга состоит в обнаружении кислотных центров на поверхности, дифференциации их типа и определении силы их кислотности. При этом в отличие от уже рассмотренных работ по исследованию окиси алюминия, на поверхности которой имеются в основном центры апротонного типа, в случае алюмосиликагелей задача значительно усложняется вследствие существования кислотных центров как с электро-яоакцепторными, так и с протонодонорными свойствами. [28]
Скорость коагуляции значительно влияет на структуру образующегося алюмосиликагеля. Сферическая форма способствует меньшему истиранию катализатора и снижает эрозию аппаратов реакторного блока, где циркулирует катализатор. [29]
Авторы смогли таким образом обнаружить в смешанных алюмосиликагелях одновременное существование двух форм кислотности, причем кислотность Льюиса появляется только после нагревания катализатора. В табл. 1 приведены результаты определений, проведенных на геле, в котором содержалось 0 1 г А1 на 100 г твердого вещества. [30]
Страницы: 1 2 3 4