Алюмосиликагель
Cтраница 4
КПЗ на поверхностях катионированных, декатионирован-ных цеолитов, алюмосиликагеля и силикагеля, однотипны по своей природе. Ими, по нашему мнению, являются кислотные центры. [46]
С самого начала работ по спектральному исследованию кислотности алюмосиликагелей ( первая работа была выполнена Мейпсом и Эйшенсом [11] в 1954 г.) была поставлена задача разработки метода идентификации кислотных центров различного типа ( Льюиса и Бренстеда) и установления различия в их активности. К настоящему времени с этой целью выполнено уже сравнительно много работ по спектральному исследованию поверхностных гидроксильных групп и самого каркаса алюмосиликагелей, а также адсорбированных молекул, причем главным образом молекул различных органических оснований. [47]
В работе [52] исследованы спектры бензальдегида, адсорбированного алюмосиликагелем при 325 С. [48]
Силихагель, активная окись алюминия, активированный глинозем и алюмосиликагель используются для восстановления масла по перко-ляциокному методу ( в термосифонах и адсорберах); отбеливающие земли используются преимущественно для востановления масел как по контактному, так и перколяционному методам. [49]
При получении бинарных гелей-катализаторов, таких как алю-моцирконий, алюмосиликагели, кроме параметров пористой структуры и величины удельной поверхности важнейшей характеристикой является степень кислотности готового ксерогеля. Если первые свойства регулируются условиями осаждения примерно также, как и у силикагеля, то кислотность поверхности определяется начальным соотношением компонентов на стадии осаждения. У всех упомянутых бинарных гелей кислотность проходит через максимум при замене части оксида кремния на оксид металла и может значительно превышать исходную кислотность чистого силикагеля. О характеристиках гелей с основными свойствами поверхности информация пока отсутствует. [50]
Для установления связи между электроноакцепторными свойствами апротонного центра поверхности алюмосиликагелей использовалась установленная в работе [40] зависимость между электроотрицательностью металла и квадратом частоты полосы поглощения координационно связанного аммиака в аммиачном комплексе. [51]
Получены зависимости, позволяющие расчетным путем подбирать условия синтеза алюмосиликагелей с заданной структурой пор. [52]
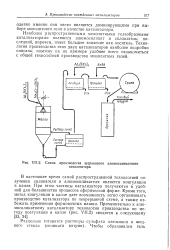 |
Схема производства шарикового алюмосиликатного. [53] |
В настоящее время самой распространенной технологией получения силикагеля и алюмосиликагеля является коагуляция в капле. При этом частицы катализатора получаются в удобной для большинства процессов сферической форме. Кроме того, метод коагуляции в капле дает возможность легко организовать производство катализатора по непрерывной схеме, а также избежать применения формовочных машин. [54]
Отсутствие в спектре обработанного при температурах выше 500 С алюмосиликагеля четкого проявления полос поглощения гидроксильных групп, аналогичных полосам поглощения гидро-ксильных групп окиси алюминия, по мнению Базила [22], свидетельствует об отсутствии на поверхности алюмосиликагеля ( содержащего менее 30 % АЬОз) участков поверхности чистой окиси алюминия. Таким образом, это указывает на довольно равномерное распределение атомов алюминия в остове алюмосиликагеля. Базила [22] считает также, что наличие в спектре одной полосы поглощения гидроксильных групп 3745 см-1 указывает на более легкое удаление гидроксильных групп, связанных с поверхностными атомами алюминия по сравнению с гидроксильными группами, связанными с поверхностными атомами кремния. Так как гидроксильные группы на поверхности чистой окиси алюминия обладают высокой термической стабильностью ( см. главу VIII), то такое различие вероятно может быть объяснено различием свойств поверхностных атомов А1 в окиси алюминия и в алюмосиликагеле. Так, предполагается [23], что атомы AI в алюмосиликагелях с низким содержанием А1 координированы тетраэдрически, в то время как в алюмосиликатных катализаторах с высоким содержанием алюминия или в чистой окиси алюминия они могут существовать в октаэдрической координации. Так, Базила [18] показал, что смещения полосы поглощения свободных гидроксильных групп при адсорбции га-ксилола и мезитилена алюмосиликагелем составляют соответственно 154 и 168 см-1, а при адсорбции кремнеземом соответственно 154 и 166 см-1. Найдено [24, 25], что величины смещения полос поглощения поверхностных гидроксильных групп при адсорбции молекул различной основности одинаковы для кремнезема и алюмосиликагеля. В работе [26] исследовано изменение интенсивности полосы поглощения свободных гидроксильных групп 3745 см-1 силикагеля и алюмосиликагеля после прокаливания в интервале температур от 25 до 600 С. [55]
Как указано выше, наблюдая избирательную адсорбцию этих молекул алюмосиликагелями, Пери [20] предположил, что на поверхности существует особый тип центров адсорбции, так называемые а-центры. Пери считает, что эти центры образуются при удалении с поверхности гидроксиль-ных групп, связанных с поверхностными атомами алюминия алюмосиликагеля. Образование поверхностных гидроксильных групп при адсорбции НС1 дегидратированным и дегидроксилировэнным алюмосиликагелем указывает, по мнению Пери, на существование на поверхности реакционноспособного иона кислорода. Подобные состояния иона кислорода не имеют места на поверхности чистых кремнеземов. [56]
Имеется указание, что пары бензола, соприкасаясь с алюмосиликагелем, дают полосы у 440 и 350 нм [3, 4], принадлежащие, очевидно, молекулярному иону, образующемуся в результате присоединения протона на поверхности этого сильно кислотного адсорбента. Впуск газообразного NH3 или диоксана устранял эти полосы. [57]
 |
Схематическая диаграмма ИК-спектров N0, адсорбированной на сочетаниях окислов. [58] |
Такие же полосы наблюдаются и в спектре N0 на алюмосиликагеле. [59]
Спектры других молекул, менее избирательно взаимодействующих с кислотными центрами алюмосиликагелей, но содержащих электронодонорные атомы кислорода и азота и способные к специфическому молекулярному взаимодействию, также свидетельствуют о сильном возмущении этих молекул при адсорбции. В работе [17] исследован спектр поглощения обертонного колебания групп СН диэтилового эфира. Найдено, что при адсорбции его из раствора в ССЦ алюмосиликагелем полоса поглощения 5765 см-1 смещается в сторону высоких частот и становится менее интенсивной. [60]
Страницы: 1 2 3 4