Ст-комплекс
Cтраница 1
Устойчивые ст-комплексы получены при взаимодействии элект-рофильных реагентов с 1, 3, 5-трис ( диметиламино) бензолом. [1]
Этот ст-комплекс имеет желтую окраску и разлагается на исходные компоненты уже при - 15 С. При использовании в качестве кислоты Льюиса SbFs вместо ВГз соль с противоионом SbFe гораздо более стабильна и не разлагается даже при 50 С. [2]
Образующийся биполярный ст-комплекс стабилизируется за счет сольватации полярным растворителем сильнее, чем менее полярным. За этот счет возрастает скорость образования о-комплекса и суммарная скорость реакции. [3]
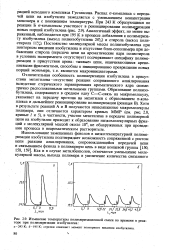 |
Изменение температуры полимеризационной смеси во времени в реакторе при полимеризации изобутилена. а - 243 К. б - 195 К. стрелки означают момент повторного введения изобутилена. [4] |
Распад ст-комплекса с передачей цепи на изобутилен замедляется с уменьшением концентрации мономера и с понижением температуры. Постоянство молекулярной массы полиизобутилена при повторном введении изобутилена и отсутствие блок-сополимера при добавлении стирола ( передача цепи на ароматические ядра полистирола в условиях эксперимента отсутствует) подчеркивают специфику полимеризации в присутствии арена: живые цепи, оканчивающиеся арено-ниевыми фрагментами, способны к инициированию превращения новых порций мономера, т.е. являются макроинициаторами. [5]
Образование ст-комплексов - ионный бимолекулярный процесс, зависящий как от реакционной способности ароматического соединения, так и от сольватационных эффектов среды. В рассматриваемом случае скорость образования ст-комплексов k слишком велика, а скорость обратной реакции 6 i слишком мала, чтобы обратная реакция могла влиять на суммарную скорость реакции. Получившийся а-комплекс является сильной кислотой и быстро, со скоростью &2, отдает свой протон основанию. [6]
Существование аналогичных ст-комплексов постулируется для объяснения реакций дейтерообмена, водородного дезалкилирования. [7]
В ст-комплексе уже имеется химическая связь, образованная за счет электронной пары из тг-системы бензола. При этом атом углерода, соседний с тем, к которому присоединилась группа NO2, лишается части своей электронной плотности и заряжается положительно. [8]
Подобного рода ст-комплексы были зафиксированы при низкой температуре для ряда других реакций электрофильного замещения в ароматическом кольце. [9]
Легкость образования ст-комплексов и связанная с ней реакционная способность ароматических соединений может быть оценена в качественной и полуколичественной форме несколькими путями, причем часто ( но, к сожалению, не всегда) они дают согласованные результаты. [10]
На стабильность ст-комплексов большое и часто даже решающее влияние оказывают заместители в ароматическом кольце. Их действие, вызывающее значительное перераспределение я-электронной плотности ароматических молекул, рассмотрено в разделе 2.4. Надо иметь в виду, что влияние заместителей в ст-комплексе может иметь существенно иной характер, чем в исходной нереагирующей молекуле. [11]
О Распад ст-комплекса на исходные компоненты протекает значительно медленнее, чем отрыв протона; тогда k2 [ B ] k и величиной kj в знаменателе можно пренебречь. [12]
Как правило, ст-комплекс неустойчив и имеет энергию, близкую к энергии истинного переходного состояния. [13]
Этот аддукт, ст-комплекс, может затем отщепить протон с образованней аниона бензолсульфокислоты. [14]
Образование изомерных 1 3-анионных ст-комплексов Сервиса делает понятным некоторые случаи аномального; так называемого кинезамещения, при котором нуклеофильный агент присоединяется не к тому атому углерода, где находилась уходящая группа. Классическим примером такого рода является реакция В. [15]
Страницы: 1 2 3 4