Ст-комплекс
Cтраница 2
В отличие от тг-комплексов ст-комплексы представляют собой истинно химические соединения, в которых электрофильный агент Х образует ковалентную связь за счет двух л-электронов одной из связей бензольного кольца. Таким образом, при образовании ст-комплек-са электрофильный агент внедряется в ароматическую молекулу более глубоко, чем в л-комплексе. [16]
В отличие от тс-комплексов ст-комплексы представляют собой истинно химические соединения, в которых электрофиль-ный агент Х образует ковалентную связь за счет двух тс-элект-ронов одной из связей бензольного кольца. Таким образом, ПРИ образовании а-комплекса электрофильный агент внедряется в ароматическую молекулу более глубоко, чем в л-комп-лексе. [17]
Стадия отщепления протона от ст-комплекса во многих случаях является быстрой. Однако в некоторых случаях, например при недостатке основания, эта стадия замедляется. Тогда наблюдается кинетический изотопный эффект водорода. В предельных, достаточно редких, случаях стадия отщепления протона может стать определяющей скорость всего процесса. [18]
У тетраэдрического атома углерода ст-комплекса находится два заместителя: один, образовавшийся из атакующего агента, другой - содержащийся в исходной молекуле. Легко понять, что успешность протекания второго этапа нуклеофильной реакции зависит от отношения скоростей отрыва этих заместителей. [19]
Стадия отщепления протона от ст-комплекса во многих случаях является быстрой. [20]
Стадия 4 - перегруппировка ст-комплекса в л-комплекс 2 продукта замещения; при этом протон отщепляется от атома углерода, у которого проходит замещение; в цикле вновь формируется ароматический секстет электронов - наблюдается реароматизация. [21]
Полагают, что образование ст-комплекса в результате присоединения протона к определенному атому углерода сопровождается переходом последнего из sp2 - в 5р3 - гибридное состояние. В соответствии с этим образующаяся С - Н связь должна быть обычной ковалентной связью. [22]
При тщательном исследовании строения анионных ст-комплексов с помощью методов, пригодных для изучения быстрых реакций, было установлено, что во многих случаях анионному 1 1-а-комплексу ( илсо-комплексу) предшествует другой, изомерный ему а-комплекс. В этом изомерном а-комплексе нуклеофиль-ный агент находится при незамещенном атоме углерода в мета-положении по отношению к уходящей группе. [23]
Перемещение алкильной группы в ст-комплексе является стадией, определяющей скорость всего процесса изомеризации. О том, как происходит это перемещение, в настоящее время судить трудно. [24]
И в этом случае первоначально образующийся ст-комплекс быстрее присоединяет нуклеофил, чем отщепляет протон, и в результате идет реакция нитроацетоксилирования. Все сказанное выше подтверждает, что вывод о течении реакций электрофнльного замещения через промежуточное образование ( т-комплексов действительно является-правильным. [25]
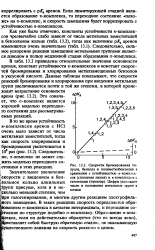
А Е соответствует энергии стабилизации ст-комплекса. [26]
Соотношение скоростей образования и распада ст-комплекса может быть различным для разных соединений, так что закономерности, обнаруженные для пентаметилбензола, нельзя распространять на другие соединения. [27]
Ниже показаны только те структуры ст-комплексов, в которых положительный заряд делокализован лишь в пиррольном цикле. [28]
Будет ли образовываться п - и ст-комплекс, зависит как от i ароматической структуры, так и от типа электрофильной час - тицы. [29]
Страницы: 1 2 3 4