Стабильность - анион
Cтраница 4
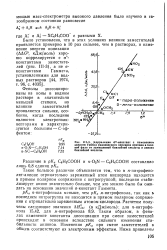 |
Корреляция а - констант с изменением энергии Гиббса равновесного переноса протона в газовой фазе от замещенной бензойной кислоты и аниону бензойной кислоты. [46] |
Ка я-нитрофенола меньше, чем рКа лг-нитрофенола, так как ь последнем нитрогруппа не находится в прямом полярном сопряжб нии с отрицательно заряженным атомом кислорода. Таким образом, в фенолах изменение константы диссоциации при смене заместителей происходит в основном вследствие сильного изменения стабильности анионов. Изменения рКа при смене заместителей в общем соответствуют их электронным эффектам. [47]
АЯ образования иона гидроксония) одинакова для всех рассматриваемых объектов. На последней стадии выигрывается энергия сольватации аннона кислоты. Энергия сольватации анионов тем больше, чем меньше делокали-зован в них отрицательный заряд атома кислорода. Следовательно, при наличии заместителей, делокализующих электронную плотность, стабильность аниона повышается, а энергия его сольватации уменьшается. [48]
С-Hal и образования связи С-Nu; на первой стадии, вероятно, образуется анион - продукт присоединения нуклеофила к реагирующей молекуле. Такие анионы имеют хи-ноидную структуру, а следовательно, яркую окраску; в их спектрах имеются характерные полосы поглощения в ИК - и видимой частях спектра. Так, при взаимодействии 2 4-динитро - 1-хлорбензола с метоксидом калия образуется окрашенный промежуточный продукт. В анионе ( 82) атомы кислорода обеих нитрогрупп в равной мере участвуют в рассредоточении полного отрицательного заряда и тем самым повышают стабильность аниона и снижают энергию активации его образования. [49]
Снижение уровня IV соответственно на столько же понижает положение уровней V и VI. Поскольку в данной главе рассматривается бренстедовская кислотность, стадия 4 ( ДЯ образования иона гидроксония) одинакова для всех рассматриваемых объектов. На последней стадии выигрывается энергия сольватации аниона кислоты. Энергия сольватации анионов тем больше, чем меньше делока-лизован в них отрицательный заряд атома кислорода. Следовательно, при наличии заместителей, оттягивающих электронную плотность, стабильность аниона повышается, а энергия его сольватации уменьшается. [50]
Дальнейшая обработка этих динуклеотидов ( выделенных в твердом состоянии в виде свободных кислот) дибензилхлорфосфатом приводит к образованию промежуточных Р1 - дибензил - Р2 - динуклео-тид-5 - пирофосфатов, гидрогенолизом которых получают динуклео-тидные производные с концевой 5 -пирофосфатной группой. Эти соединения, вероятно, интересны с точки зрения действия на них поли-нуклеотидфосфорилазы. Другой метод синтеза аналогичных соединений состоит в обработке дибензилпроизводного ( или Ра-дифе-нил Р2 - динуклеотид-5 - пирофосфата, получающегося при действии дифенилхлорфосфата) фосфорной кислотой, замещающей в результате нуклеофильной атаки дибензил ( или дифенил) фосфорную группу. Следует отметить, что при данных условиях хлорфосфаты реагируют только со вторичной гидроксильнои группой фосфатного остатка ( иначе наблюдался бы разрыв межнуклеотидной связи) и что при анионном обмене снова более устойчивый анион вытесняется менее устойчивым. Факт, что предпочтительной реакцией является взаимодействие вторичной гидроксильнои группы, уже обсуждался при описании действия на аналогичные соединения этилового эфира хлоругольной кислоты; эта специфичность обусловливается значительным различием в стабильности первичных и вторичных фосфорильных анионов. [51]
Степень иопности связи металл-лиганд зависит от: лектроотрицатель-ности атомов или групп, входящих в нее и, в частности, зависит от стабильности аниона р-дикетона. Чем более стабильный анион образует Р - ДИКОТОН, тем более лонная связь металл - лиганд должна образоваться. В свою очередь стабильность аниона р-дикетона зависит от степени делокализации отрицательного заряда по молекуле. Чем больше он делокализован по большему числу атомов и групп, тем стабильнее анион. Отсюда видна роль заместителей в р-дикетоне в долокализации заряда в анионе. При этом допорпые заместители сильнее локализуют отрицательный заряд на атомах кислорода, уменьшая стабильность аниона, а акцепторы электронов, способствуя делокализации отрицательного заряда, увеличивают стабильность аниона по сравнению с нейтральным заместителем, за какой обычно принимают метил. [52]
Степень иопности связи металл-лиганд зависит от: лектроотрицатель-ности атомов или групп, входящих в нее и, в частности, зависит от стабильности аниона р-дикетона. Чем более стабильный анион образует Р - ДИКОТОН, тем более лонная связь металл - лиганд должна образоваться. В свою очередь стабильность аниона р-дикетона зависит от степени делокализации отрицательного заряда по молекуле. Чем больше он делокализован по большему числу атомов и групп, тем стабильнее анион. Отсюда видна роль заместителей в р-дикетоне в долокализации заряда в анионе. При этом допорпые заместители сильнее локализуют отрицательный заряд на атомах кислорода, уменьшая стабильность аниона, а акцепторы электронов, способствуя делокализации отрицательного заряда, увеличивают стабильность аниона по сравнению с нейтральным заместителем, за какой обычно принимают метил. [53]
Страницы: 1 2 3 4