Стадия - зарождение - цепь
Cтраница 4
Если в системе в небольших концентрациях образуются свободные радикалы, to они преимущественно реагируют с молекулами реагентов с сохранением свободной валентности. Несколько таких последовательных реакций могут привести к регенерации исходного свободного радикала и затем к многократному повторению того же цикла превращений - цепному процессу. Продукты реакции образуются на стадиях продолжения цепи, первичные свободные радикалы появляются на стадии зарождения цепи. Побочные реакции, приводящие к исчезновению свободной валентности, называются обрывом цепей. Если в ходе развития цепи происходит нарастание числа свободных радикалов, то цепной процесс называют рааветвленным. Для таких, процессов характерны предельные ( критические) явления - - переход в узком диапазоне условий от медленного к быстрому ускоренному развитию - цепному воспламенению. [46]
Благодаря этому та же последовательность элементарных реакций может повториться вновь, затем еще и еще, пока свободный радикал не исчезнет по той или иной причине. Таким образом и осуществляется цепной процесс, в котором один радикал, образовавшийся на стадии зарождения цепи, приводит к образованию многих молекул продукта В. [47]
Во второй реакции образовался тот же свободный радикал Y -, с которого началось превращение. Благодаря этому последовательность элементарных реакций может повториться вновь, затем еще и еще, пока свободный радикал не исчезнет по той или иной причине. Таким образом и осуществляется цепной процесс, в котором один радикал, образовавшийся на стадии зарождения цепи, приводит к образованию многих молекул продукта В. [48]
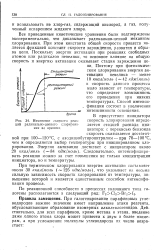 |
Изменение. скорости реакций. радикально-цепного хлорирования во времени. [49] |
Все приведенные кинетические уравнения были подтверждены экспериментально, что доказывает радикально-цепной механизм хлорирования. При этом константа общей скорости процесса является функцией констант скорости зарождения, развития и обрыва цепи. Поскольку энергии активации при реакциях свободных атомов или радикалов невелики, то основное влияние на общую скорость и энергию активации оказывает стадия зарождения цепи. Поэтому при фотохимическом хлорировании энергия активации невелика - менее 10 ккал / моль ( - 42 кдж / моль) и скорость данного процесса мало зависит от температуры, что определяет возможность его проведения при низких температурах. [50]
Термическое хлорирование в боковую цепь ароматических углеводородов сопровождается разложением продуктов реакции. Например, хлорированием толуола в газовой фазе получают бензилхлорид с умеренным выходом. При фотохимическом хлорировании источником света может быть солнечный или рассеянный дневной свет, ртутная лампа, видимые ультрафиолетовые лучи с длиной волны более 300 нм. Температура фотохимического хлорирования ароматических углеводородов должна быть не ниже 100 С, чтобы избежать возможного замещения в ароматическом кольце. Нежелательно присутствие даже минимальных количеств кислорода, ввиду его ингибирующего действия, а также любых других соединений, способных катализировать реакцию хлорирования в ароматическое кольцо. Лимитирующей стадией фотохлорирования является стадия зарождения цепи. [51]
Страницы: 1 2 3 4