Стадия - продолжение - цепь
Cтраница 2
В пользу участия комплексов никеля в стадии продолжения цепи свидетельствует прямая пропорциональная зависимость дапр. [16]
Если возбужденная молекула, образовавшаяся в сильно экзотермической стадии продолжения цепи, не может распасться с образованием свободных атомов или радикалов, то разветвление все же может произойти в результате передачи энергии возбуждения другой молекуле. [17]
Эффект соседа может проявляться на обеих стадиях продолжения цепи. [18]
При этом ион металла-катализатора начинает участвовать в стадии продолжения цепи, а его роль в вырожденном разветвлении цепи становится менее существенной. [19]
Относительная концентрация радикалов зависит от относительных скоростей стадий продолжения цепей. [20]
Цепные реакции, в которых стадия инициирования, стадия продолжения цепи или и та, и другая происходят каталитически, называют цепно-каталитическими. [21]
 |
Кинетика накопления гидроперекиси в реакции. [22] |
Реакция ( 4а) учитывает участие катализатора в стадии продолжения цепи. [23]
Лимитирующая роль реакции ацильного радикала с кислородом на стадии продолжения цепи отмечается также при окислении метакролеина [127], и в большинстве случаев скорость окисления алифатических ненасыщенных альдегидов [127, 143, 147, 194] имеет первый порядок по кислороду. Различная реакционная способность насыщенных и ненасыщенных альдегидов ( при окислении) связана [127] с тем, что константа скорости взаимодействия ацильного радикала с кислородом значительно меньше для радикалов, образующихся из ненасыщенных альдегидов, поэтому последние окисляются медленнее, чем насыщенные. Метакролеин и акролеин окисляются примерно с одинаковой скоростью, что говорит о незначительном эффекте х - СН3 группы, в то время как значительное увеличение скорости окисления кретонового альдегида ( - в 7 раз) указывает на существенное влияние ( 3-заме-щения. [24]
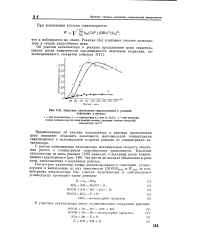 |
Кинетика накопления гидроперекиси в реакции окисления н. декана. [25] |
Реакция ( 4а) учитывает участие катализатора в стадии продолжения цепи. [26]
Дальнейшие исследования позволили обнаружить цепной окислительно-восстановительный процесс, в стадиях продолжения цепи которого не только не образуется свободных субстратных радикалов, но и не происходит изменения валентного состояния иона металла. [27]
При достаточно большой длине цепи, как мы видели раньше, скорости стадий продолжения цепи равны. Это означает, что скорости расходования и образования радикалов на стадиях продолжения цепи одинаковы. [28]
Из приведенных данных следует, что скорость реакции окисления углеводорода, контролируемая стадией продолжения цепи, зависит, с одной стороны, от активности пероксидного радикала, с другой - от энергии разрыва связи и пространственных особенностей С - Н - связи в окисляющемся углеводороде. В зависимости от строения углеводорода, а также от условий проведения реакции, например, при замене одного окислителя ( кислорода) другим ( переходным металлом в высшей валентной форме) вклад электронных факторов и термодинамической стабильности радикалов ( катион-радикалов) может существенно-меняться. [29]
Для селективного окисления углеводородов в ти-дроперокси-ды необходимо, чтобы гидропероксидное направление реакции на стадии продолжения цепи ( реакция 1.3) было преобладающим не менее чем на порядок по скоростям реакций, что может быть достигнуто при низких концентрациях катализатора в зависимости от характера среды и природы иона металла. [30]
Страницы: 1 2 3 4