Макроскопическая стадия
Cтраница 2
Представления о макроскопических стадиях цепных реакций и об особой роли начального периода, разработанные Эмануэлем373, предусматривают возможность появления начальных инициирующих продуктов, возникновение которых может подавляться ингибитором. В случае, если они все-таки образуются, возможно и такое положение, когда ингибитор уже не сможет предотвратить цепную реакцию. Предложены уравнения, описывающие ингибирование неразветвленных и разветвленных цепных реакций с учетом влияния дополнительного обрыва цепи. [16]
На этом заканчивается первая макроскопическая стадия процесса. [17]
Представление о существовании макроскопических стадий и особой роли начального периода побуждает нас поднять вопрос о развитии новых рациональных приемов проведения цепных химических реакций. Само собой разумеется, что разные макроскопические стадии будут по-разному относиться к заданным условиям. Совсем не обязательно, чтобы условия, благоприятные для осуществления начальных инициирующих стадий, были бы оптимальными и для последующих стадий, индуцированных начальной. [18]
Была показана распространенность макроскопических стадий в различных цепных процессах. Наличие этих стадий усложняет классическую картину протекания неразветвленных и разветвленных цепных процессов. Появляются дополнительные возможности управления цепными реакциями: воздействие на макроскопические стадии путем изменения условий протекания процесса на различных его стадиях. [19]
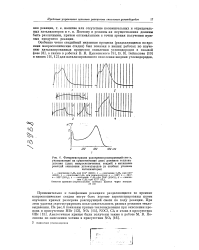
При наличии двух макроскопических стадий, каждая из которых имеет свое значение теплового эффекта и свою область максимальной скорости, суммарная зависимость аТ от времени изображается кривой с двумя налагающимися друг на яруга максимумами. Для иллюстрации на рис. 101 приведена кривая разогрева в реакции окисления пропана в присутствии НВг, которая, как указывалось, состоит из двух макроскопических стадий. [20]
 |
Изменение валентности Ni в решетке NiO под влиянием одно - и трехвалентных катионов. [21] |
Структурообразующие - регулирующие скорость макроскопических стадий в основном путем изменения структуры и величины удельной поверхности. [22]
Этот запрет относится к макроскопическим стадиям процесса, но не к молекулярным актам, не ограниченным вторым началом. Поэтому детальная траектория движения вектора и будет проходить не точно по поверхности конуса энергии, а заходить в макроскопически запрещенную область в пределах, соизмеримых с би. Эта задача подобна той, которая решается в теории флюктуации, и здесь ее можно не касаться. [23]
Быстрым и показательным методом обнаружения макроскопических стадий в сложной реакции является метод разогрева, описанный подробно в гл. Метод основан на измерении разности температур аТ в центре и на стенке реакционного сосуда, возникающей в ходе экзотермической реакции в результате разогрева реакционной смеси. Эта разность температур, как впоследствии будет показано, пропорциональна скорости реакции и ее тепловому эффекту. [24]
В одной из статей сборника рассматриваются макроскопические стадии, обнаруженные при изучении жидкофазного окисления бутана в металлическом реакторе. Сообщенные в этой статье результаты представляют определенный интерес, поскольку в настоящее время в СССР осваивается промышленное производство уксусной кислоты и других продуктов на основе этой реакции. [25]
При исследовании кинетических закономерностей, присущих отдельным макроскопическим стадиям сложного процесса окисления углеводородов, используют несколько различных методов и приемов, позволяющих изучать данную стадию реакции изолированно ох всей остальной системы. [26]
При исследовании кинетических закономерностей, присущих отдельным макроскопическим стадиям сложного процесса окисления углеводородов, используют несколько различных методов и приемов, позволяющих изучать данную стадию реакции изолированно от всей остальной системы. [27]
Применительно к газофазным реакциям разделяющиеся во времени макроскопические стадии могут быть хорошо зарегистрированы путем изучения кривых разогрева реагирующей смеси по ходу реакции. При этом удается зарегистрировать последовательность разных режимов тепловыделения. [29]
На рис. 5 приводится пример изучения одной макроскопической стадии - инициированного окисления а-фенилэтилгидроперекиси, а именно: накопление спирта в ходе этой реакции. [30]
Страницы: 1 2 3 4